题目内容
0.02mol·L—1的HCN溶液与0.02mol·L—1的NaCN溶液等体积混合,已知混合溶液中C(CN—)<C(Na+),则下列关系中,正确的是:
- A.C(Na+)>C(CN—)>C( H+)>C(OH―)
- B.C(HCN)+C (CN—)=0.04mol·L—1
- C.C(Na+)+C(H+)= C(CN—)+C(OH―)
- D.C(CN—)>C(HCN)
C
试题分析:A项不符合溶液中的电荷守恒;B项中,由于两种溶液是等体积等溶度混合的,故溶度没有变化,为0.02mol·L—1;C项满足溶液中电荷守恒,故选择C项。
考点:溶液中电离平衡以及物料守恒。
点评:本题属于弱酸与弱酸强碱盐混合型题目,注意使用电荷守恒与物料守恒来分析。
试题分析:A项不符合溶液中的电荷守恒;B项中,由于两种溶液是等体积等溶度混合的,故溶度没有变化,为0.02mol·L—1;C项满足溶液中电荷守恒,故选择C项。
考点:溶液中电离平衡以及物料守恒。
点评:本题属于弱酸与弱酸强碱盐混合型题目,注意使用电荷守恒与物料守恒来分析。

练习册系列答案
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
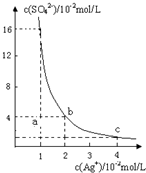 某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:
某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示: