题目内容
已知8gA能与32gB恰好完全反应,生成22gC和一定量D,现将16gA与70gB的混合物充分反应后,生成2mol D和一定量的C,则D的摩尔质量为多少?
考点:化学方程式的有关计算
专题:计算题
分析:8gA能与32gB恰好完全反应,生成22gC和一定量D,根据质量守恒,生成D的质量为8g+32g-22g=18g,故A、B、C、D按质量比8g:32g:22g:18g=4:16:11:9进行反应,据此进行16gA与70gB反应的过量计算,再根据质量比计算生成的D的质量,利用M=
计算D的摩尔质量.
| m |
| n |
解答:
解:8gA能与32gB恰好完全反应,生成22gC和一定量D,根据质量守恒D的质量为8g+32g-22g=18g,故A、B、C、D按质量比8g:32g:22g:18g=4:16:11:9进行反应,16gA完全反应需要B的质量为16g×
=64g<70g,故B过量,则生成的D的质量为16g×
=36g,故D的摩尔质量为
=18g/mol,
答:D的摩尔质量为18g/mol.
| 16 |
| 4 |
| 9 |
| 4 |
| 36g |
| 2mol |
答:D的摩尔质量为18g/mol.
点评:本题考查化学方程式计算、摩尔质量计算,比较基础,关键是利用质量守恒定律确定反应中各物质的质量定比关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应的离子方程式书写正确的是( )
| A、NaHCO3的水解:HCO3-+H2O?H3O++CO32- | ||||
| B、硫酸亚铁溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+=2Fe3++2H2O | ||||
| C、硫酸铜溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓ | ||||
D、除去KNO3溶液中的Fe3+:Fe3++3H2O
|
若(NH4)2SO4在强热时分解的产物是SO2、N2、NH3和H2O,则该反应产物中SO2和NH3的物质的量之比为( )
| A、1:4 | B、3:4 |
| C、4:1 | D、4:3 |
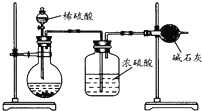 为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案: