题目内容
1.下列指定反应的离子方程式正确的是( )| A. | 氯气溶于水:Cl2+H2O=2H++Cl-+ClO- | |
| B. | Na2CO3溶液中CO32-的水解:CO32-+H2O=HCO3-+OH- | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+=I2+3H2O | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O |
分析 A.氯气与水生成HClO,HClO为弱酸,应写成化学式;
B.CO32-的水解为可逆反应;
C.电荷不守恒;
D.NaHCO3溶液中加足量Ba(OH)2溶液,生成BaCO3和水.
解答 解:A.氯气溶于水,反应的离子方程式为Cl2+H2O?H++Cl-+HClO,HClO为弱酸,应写成化学式,且为可逆符号,故A错误;
B.CO32-的水解为可逆反应,应为CO32-+H2O?HCO3-+OH-,故B错误;
C.酸性溶液中KIO3与KI反应生成I2,发生IO3-+5I-+6H+=3I2+3H2O,故C错误;
D.NaHCO3溶液中加足量Ba(OH)2溶液,生成BaCO3和水,发生HCO3-+Ba2++OH-=BaCO3↓+H2O,故D正确.
故选D.
点评 本题为2015年江苏卷第9题,考查了离子方程式的判断,为常见题型,侧重于学生的分析能力以及元素化合物知识的综合理解和运用的考查,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等,难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
16.在CO2中,Mg燃烧生成MgO和C.下列说法正确的是( )
| A. | 元素C的单质只存在金刚石和石墨两种同素异形体 | |
| B. | Mg、MgO中镁元素微粒的半径:r(Mg2+)>r(Mg) | |
| C. | 在该反应条件下,Mg的还原性强于C的还原性 | |
| D. | 该反应中化学能全部转化为热能 |
1.下列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
x?Y
x?Y
| 物质 选项 | X | Y |
| A | Na2CO3 | NaHCO3 |
| B | Al(OH)3 | Al2O3 |
| C | FeCl3 | FeCl2 |
| D | CuSO4 | Cu(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
2.下列溶液中粒子的物质的量浓度关系正确的是( )
| A. | 20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| B. | 0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(H+)+c(Cl-)>c(NH4+)+c(OH-) | |
| D. | 0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |






 (或
(或
 );
);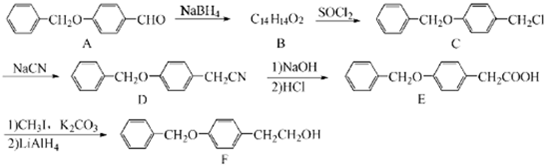
 ;由C→D的反应类型是:取代反应.
;由C→D的反应类型是:取代反应. .
. 为原料制备化合物X(结构简式见图)的合成路线流程图(无机试剂可任选).合成路线流程图示例如图:CH3CHO$→_{催化剂△}^{O_{2}}$CH3COOH$→_{浓硫酸△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
为原料制备化合物X(结构简式见图)的合成路线流程图(无机试剂可任选).合成路线流程图示例如图:CH3CHO$→_{催化剂△}^{O_{2}}$CH3COOH$→_{浓硫酸△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
