题目内容
四种短周期元素X、Y、Z、W,原子序数依次增大,请结合表中信息回答下列问题。

(1)W元素在周期表的位置为______________。
(2)上述元素的最高价氧化物对应的水化物中,有一种物质与其它三种物质在一定条件下均能发生化学反应,该元素是_________(填元素名称)。
(3)X元素的最高价氧化物对应的水化物与其气态氢化物反应得到的化合物为___________(填化学式)。
(4)向含有Z元素的简单阳离子的溶液中加入过量的NaOH溶液,发生反应的离子方程式为_____________________________________。
(5)下列可作为比较Z和Mg金属性强弱的方法是_______(填代号)。
a.测两种元素单质的硬度和熔、沸点
b.测等浓度相应氯化物水溶液的pH
c.比较单质与同浓度盐酸反应的剧烈程度
d.比较两种元素在化合物中化合价的高低
(6)Z单质和Mg组成的混合物是一种常见的焰火材料,某化学兴趣小组设计了如下图所示的实验方案,测定该混合物中Z的质量分数。
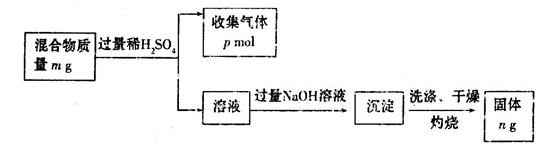
能确定混合物中Z的质量分数的数据组有_________(填代号)。
a.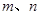 b.
b.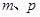 c.
c.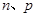

(1)W元素在周期表的位置为______________。
(2)上述元素的最高价氧化物对应的水化物中,有一种物质与其它三种物质在一定条件下均能发生化学反应,该元素是_________(填元素名称)。
(3)X元素的最高价氧化物对应的水化物与其气态氢化物反应得到的化合物为___________(填化学式)。
(4)向含有Z元素的简单阳离子的溶液中加入过量的NaOH溶液,发生反应的离子方程式为_____________________________________。
(5)下列可作为比较Z和Mg金属性强弱的方法是_______(填代号)。
a.测两种元素单质的硬度和熔、沸点
b.测等浓度相应氯化物水溶液的pH
c.比较单质与同浓度盐酸反应的剧烈程度
d.比较两种元素在化合物中化合价的高低
(6)Z单质和Mg组成的混合物是一种常见的焰火材料,某化学兴趣小组设计了如下图所示的实验方案,测定该混合物中Z的质量分数。

能确定混合物中Z的质量分数的数据组有_________(填代号)。
a.
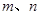 b.
b.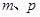 c.
c.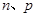
(1)第三周期 第ⅣA族(2分)
(2)钠(2分)
(3)NH4NO3 (2分)
(4)Al3++4OH-=[Al(OH)4]- (2分)
(5)bc (2分)
(6)abc (2分)
(2)钠(2分)
(3)NH4NO3 (2分)
(4)Al3++4OH-=[Al(OH)4]- (2分)
(5)bc (2分)
(6)abc (2分)
试题分析:由表中信息可得X为N,Y为Na,Z为Al,W为Si。
(1)Si在元素周期表的位置为第三周期 第ⅣA族。
(2)氢氧化钠可以和硝酸、氢氧化铝、硅酸均可以反应。
(3)氨气和硝酸反应:NH3++HNO3=NH4NO3.
(4)略
(5)金属性强弱的方法有:比较最高价氧化物对应水化物的碱性强弱,比较置换出氢的难易程度,另外比较等浓度相应氯化物水溶液的pH也可以,pH越小,金属性越弱。
(6)a.
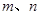 w =1-(3n)/(5m)
w =1-(3n)/(5m)b.
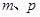 设Al的物质的量为x,Mg的物质的量为y,则y+3x/2=p,27x+24y=m,可解得x,y。就可以求出Z的质量分数。
设Al的物质的量为x,Mg的物质的量为y,则y+3x/2=p,27x+24y=m,可解得x,y。就可以求出Z的质量分数。c.
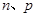 设Al的物质的量为x,Mg的物质的量为y,y+3x/2=p,40y=n。可解得x,y。就可以求出Z的质量分数
设Al的物质的量为x,Mg的物质的量为y,y+3x/2=p,40y=n。可解得x,y。就可以求出Z的质量分数
练习册系列答案
相关题目

