题目内容
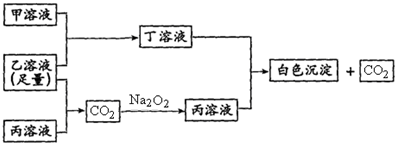
有A、B、C三种常见的短周期元素,它们的原子序数逐渐增大,B元素原子最外层电子数是C元素原子最外层电子数的一半,A元素最外层电子数比B多一个。甲、乙、丙是3种含氧酸的钠盐,甲中含B元素,乙中含C元素,丙中含A元素,甲、丙溶液pH>7,乙溶液pH<7;丁为气体,戊为淡黄色固体。甲、乙、丙、丁、戊、己六种物质之间的相互反应关系如下图:?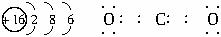
请回答:?
(1)写出C元素的原子结构示意图,写出丁和戊的电子式_________、________;丁在固态时属于___________晶体。
(2)用有关化学用语解释:
①乙溶液呈酸性的原因____________________;
②丙溶液呈碱性的原因____________________。
(3)写出有关反应的离子方程式:?
①乙溶液+丙溶液→丁__________________;?
②己溶液+丙溶液→丁__________________。?
(1)![]()
![]()
(2)①HSO![]() ══H ++SO
══H ++SO![]() ,?
,?
②CO![]() +H2O
+H2O![]() HCO
HCO![]() +OH -
+OH -
(3)①2H ++CO![]() ══CO2↑+H2O
══CO2↑+H2O
②2Al 3++3CO![]() +3H2O══2Al(OH)3↓+3CO2↑
+3H2O══2Al(OH)3↓+3CO2↑
解析:此题关键推出A、B、C三种元素,因A、B、C均可形成钠盐,故非金属性较强,最外层电子数一般大于3个(铝为3个)。因B最外层电子数为C的一半,C最外层电子数只能为6个,可推知为S。则B为Al或B,A为碳酸硅。因A的原子序数小于B,故B只能为Al,A只能为碳,由此确定出A为碳,B为铝,C为硫。?
然后利用甲、乙、丙间的转化关系,据pH和状态、颜色可推出每一种物质。

练习册系列答案
相关题目