题目内容
用20 mL FeCl3溶液腐蚀3.2 g Cu片,将Cu片完全腐蚀后,加入铁粉2.8g ,反应后溶液中存在不溶物1.6g(设反应前后溶液体积变化忽略不计)。
计算:⑴20 mL这种溶液中的FeCl3与多少毫升5 mol•L-1的FeCl3溶液中所含FeCl3的物质的量相等?
⑵反应后溶液中Fe2+的物质的量浓度为多少?
解析:
⑴V( ⑵c(
|
提示:
在该反应中Fe、Cu都是还原剂,被腐蚀的Cu为0.05 mol,投入的Fe粉也为0.05 mol,因此铁粉只可能恰好完全反应或不足,最后剩余的1.6 g不溶物一定为铜。由于Fe3+得电子数等于Fe和Cu的失电子总数, 则:n(Fe3+)=2×n(Fe)+2×n(Cu)= ⑴由于两种溶液中溶质的物质的量相等,则5 mol•L-1的FeCl3溶液的体积V( ⑵2Fe3+ + Cu = 2Fe2+ + Cu2+ 2 mol 1 mol 2 mol 0.1 mol 0.05 mol n1 2Fe3+ + Fe == 2 Fe2+ 2mol 1mol 3mol (0.15-0.1)mol 0.25mol n2 Fe + Cu2+ == Fe2+ + Cu 1mol 1mol
所以溶液中n(Fe2+)= n1+ n2+ n3=0.1 mol+0.075 mol+0.025 mol=0.2 mol, c( 也可以根据溶液中电荷守恒来计算:2n(Fe2+)+2n(Cu2+)=n(Cl-) n(Fe2+)= c( 或根据铁元素质量守恒计算: n(Fe2+)= n(Fe3+)+ n(Fe)=0.15
mol+ c(
|

分别用20 mL 1mol/L BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是( )
| A.3∶2∶2 | B.1∶2∶3 | C.1∶3∶3 | D.3∶1∶1 |
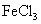 =0.15 mol。
=0.15 mol。