题目内容
下列解释实验现象的反应方程式不正确的是
- A.新制氯水中滴加NaOH溶液后,黄绿色褪去Cl2+2OH-=Cl-+ClO-+H2O
- B.向NaHCO3 溶液中滴加酚酞溶液,溶液变红HCO3-?H++CO32-
- C.向Mg(OH)2悬浊液中滴加FeCl3溶液,生成红褐色沉淀3Mg(OH)2+2Fe3+=2Fe(OH)3↓+3Mg2+
- D.向少量苯酚稀溶液中逐滴加入饱和溴水,生成白色沉淀
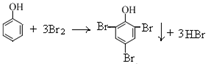
分析:A、新制氯水中滴加NaOH溶液后,氯气和氢氧化钠溶液反应生成氯化钠次氯酸钠和水;
B、碳酸氢根离子水解显碱性;
C、氯化铁水解显酸性能溶解氢氧化镁,促进铁离子水解,生成氢氧化铁沉淀;
D、苯酚和浓溴水发生取代反应反应生成白色沉淀;
解答:A、新制氯水中滴加NaOH溶液后,黄绿色褪去,是氯气和氢氧化钠反应,反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O;故A正确;
B、向NaHCO3 溶液中滴加酚酞溶液,溶液变红是因为碳酸氢根离子水解显碱性,反应的离子方程式为:H2O+HCO3-?OH-+H2CO3 ;故B错误;
C、向Mg(OH)2悬浊液中滴加FeCl3溶液,生成红褐色沉淀,反应的离子方程式为:3Mg(OH)2+2Fe3+=2Fe(OH)3↓+3Mg2+;故C正确;
D、向少量苯酚稀溶液中逐滴加入饱和溴水,生成白色沉淀,反应的化学方程式为;
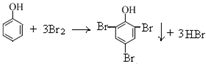 ,故D正确;
,故D正确;故选B.
点评:本题考查了反应离子方程式的正误分析,书写方法,掌握反应实质是解题关键,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | --- |
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是
(3)实验室溶解该熔融物,下列试剂中最好的是
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液

Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.为了测定熔融物中两种金属的物质的量之比,某同学取一定量上述的熔融物与足量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
(1)逐滴加入4mol/L的氢氧化钠溶液的定量玻璃仪器
(2)由上述图形分析可知,溶液中结合OH-能力最强的离子是
(3)通过如图数据试计算,熔融物中两种金属的物质的量之比n(Fe):n(Al)=
 某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | -- |
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是
(3)实验室溶解该熔融物,下列试剂中最好的是
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.则B点对应的沉淀的物质的量为
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | -- |
(填“合理”或“不合理”)
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是
反应的离子方程式为
(3)实验室溶解该熔融物,下列试剂中最好的是
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
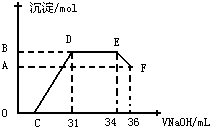
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为
(2)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为
(3)B点对应的沉淀的物质的量为
物 质 | Al | Al2O3 | Fe | Fe2O3 |
熔点/℃ | 660 | 2 054 | 1 535 | 1 462 |
沸点/℃ | 2 467 | 2 980 | 2 750 | — |
I.(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理?答:___________(填“合理”或“不合理”)。
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中是否含有金属铝。该实验所用试剂是_____________,可能发生反应的离子方程式为______________________________。
(3)实验室溶解该熔融物,下列试剂中最好的是___________(填序号)。
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4 mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积 (mL)与产生的沉淀的物质的量(mol)的关系如下图所示。试回答下列问题:

(4)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为______________________。
(5)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为_____________;上述现象说明溶液中____________结合OH-的能力比__________强(填离子符号)。
(6)B与A的差值为_________mol。
(7)B点对应的沉淀的物质的量为____________mol,C点对应的氢氧化钠溶液的体积为___________mL。
 由短周期元素组成的10种物质A~J之间有下图关系.已知:A、B为同周期相邻元素的单质,其余均为化合物;通常情况下A为固体,B、D为气体且B呈黄绿色,F为液体,A和G的浓溶液加热时反应生成D和F,J在光照时有I生成.
由短周期元素组成的10种物质A~J之间有下图关系.已知:A、B为同周期相邻元素的单质,其余均为化合物;通常情况下A为固体,B、D为气体且B呈黄绿色,F为液体,A和G的浓溶液加热时反应生成D和F,J在光照时有I生成.
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O