题目内容
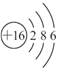
X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7。回答下列问题:(1)元素X氢化物的电子式为____________。
(2)元素Y的一种同位素可测定文物年代,这种同位素的符号是____________。
(3)元素Z能与氢元素形成一价阴离子,该阴离子的电子总数是____________。
(4)元素W与元素X相比,非金属性较强的是____________(用元素符号表示),下列表述中能证明这一事实的是____________。
①常温下W的单质和X的单质状态不同
②W的氢化物比X的氢化物稳定
③一定条件下W和X的单质都能与氢氧化钠溶液反应
(5)探寻物质的性质差异性是学习的重要方法之一。X、Y、Z、W四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是____________(用酸的分子式表示),理由是_________________________________________。
(1)![]() (2)
(2)![]() 或
或
(3)10 (4)Cl ② (5)H2CO3 只有碳酸是弱酸,其余酸均为强酸
解析:由题意知X、Y、Z、W为1—3周期元素。由X原子M层上的电子数是原子核外电子层数的2倍可推知X为16号元素硫(S);由Y原子最外层电子数是次外层电子数的2倍可推知Y为碳元素(C);由Z的单质为双原子分子,其氢化物水溶液呈碱性可推知Z为氮元素(N);由W元素的最高正价是+7价,可知W为氯元素(Cl),所以X的氢化物为H2S,其电子式为![]() 。C元素的同位素
。C元素的同位素![]() 可用于测定文物的年代。N与H元素形成的-1价阴离子为
可用于测定文物的年代。N与H元素形成的-1价阴离子为![]() ,其电子总数为10。Cl的非金属性比S的强,可通过HCl比H2S更稳定来证明,与常温下其单质的状态及二者都能在一定条件下与NaOH溶液反应无关。X、Y、Z、W四种元素最高价氧化物对应的水化物依次为H2SO4、H2CO3、HNO3、HClO4,其中只有H2CO3为弱酸,其余均为强酸。
,其电子总数为10。Cl的非金属性比S的强,可通过HCl比H2S更稳定来证明,与常温下其单质的状态及二者都能在一定条件下与NaOH溶液反应无关。X、Y、Z、W四种元素最高价氧化物对应的水化物依次为H2SO4、H2CO3、HNO3、HClO4,其中只有H2CO3为弱酸,其余均为强酸。

 名校课堂系列答案
名校课堂系列答案