题目内容
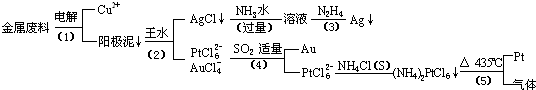
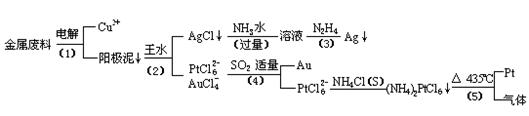
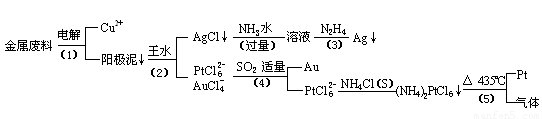
从含银、铜、金和铂的金属废料中提取金、银、铂的一种工艺如下:
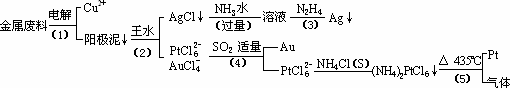
根据以上工艺回答下列问题:
(1)电解时,以金属废料为阳极,纯铜为阴极,CuSO4溶液为电解液,写出电解方程式:
阳极:________
阴极:________;
(2)AgCl溶于氨水后所得的溶液含有的一种阳离子,在碱性条件下,也可用葡萄糖将其还原为银,写出该反应的离子方程式:________;
(3)写出步骤(4)的离子反应方程式:________;
(4)金和浓硝酸反应的化学方程式为:
Au+6HNO3(浓)![]() Au(NO3)3+3NO2↑+3H2O
Au(NO3)3+3NO2↑+3H2O
但该反应的平衡常数很小,所以金和浓硝酸几乎不反应,但金却可以溶于王水,试简要解释之:________.
答案:
解析:
解析:
|
(1)Cu-2e―→Cu2+ Cu2++2e-→Cu(各1分) (2)2Ag(NH3)2++2OH-+CH2OH(CHOH)4CHO→2Ag+4NH3+CH2OH(CHOH)4COOH+H2O(3分) (3)2AuCl4-+3SO2+6H2O (4)王水中含有大量的Cl-,Au3+与Cl-可生成AuCl4-,使该平衡中Au3+浓度降低,平衡正移,金即可溶于王水.(3分) |

练习册系列答案
相关题目

 2Ag+4NH3+CH2OH(CHOH)4COOH+H2O
2Ag+4NH3+CH2OH(CHOH)4COOH+H2O