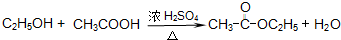题目内容
在①CH2=CH2;②C6H6;③CH3CH2OH;④CH3COOH;⑤聚乙烯五种物质中:(1)能使Br2的CCl4溶液褪色的是
(2)属于高分子化合物的是
(3)能与Na2CO3溶液反应的是
(4)能发生酯化反应的是
(5)既能发生取代反应又能发生加成反应的是
分析:(1)与溴发生反应的物质能够使溴水褪色;
(2)相对分子量达到10000以上的化合物为高分子化合物;
(3)含有羧基的有机物能够与碳酸钠溶液反应;
(4)含有羟基或者羧基的反应能够发生酯化反应;
(5)含有碳碳双键或者苯环的物质能够发生加成反应,烷烃或苯、苯的同系物能够发生取代反应.
(2)相对分子量达到10000以上的化合物为高分子化合物;
(3)含有羧基的有机物能够与碳酸钠溶液反应;
(4)含有羟基或者羧基的反应能够发生酯化反应;
(5)含有碳碳双键或者苯环的物质能够发生加成反应,烷烃或苯、苯的同系物能够发生取代反应.
解答:解:(1)①CH2=CH2分子中含有碳碳双键,能够是溴的四氯化碳溶液褪色,
故答案为:①;
(2)⑤聚乙烯为乙烯通过加成反应生成的高分子化合物,
故答案为:⑤;
(3)④CH3COOH中含有羧基,酸性强于碳酸,能够与碳酸钠溶液反应生成乙酸钠、二氧化碳和水,
故答案为:④;
(4)③CH3CH2OH、④CH3COOH中分别含有羟基、羧基,能够发生酯化反应,
故答案为:③④;
(5)②C6H6为苯,能够与氢气发生加成反应,能够在溴化铁做催化剂的条件下与液溴发生取代反应,
故答案为:②.
故答案为:①;
(2)⑤聚乙烯为乙烯通过加成反应生成的高分子化合物,
故答案为:⑤;
(3)④CH3COOH中含有羧基,酸性强于碳酸,能够与碳酸钠溶液反应生成乙酸钠、二氧化碳和水,
故答案为:④;
(4)③CH3CH2OH、④CH3COOH中分别含有羟基、羧基,能够发生酯化反应,
故答案为:③④;
(5)②C6H6为苯,能够与氢气发生加成反应,能够在溴化铁做催化剂的条件下与液溴发生取代反应,
故答案为:②.
点评:本题考查了有机物结构与性质、有机反应类型判断,题目难度中等,注意掌握常见有机物的结构与性质,明确常见的烃的衍生物官能团与反应类型之间的关系.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目