题目内容
阿波罗宇宙飞船上使用的是氢-氧燃料电池,其电极总反应式为:2H2+O2=2H2O;电解质溶液为KOH溶液,反应保持在较高温度,使水蒸发,下列叙述正确的是
- A.此电池能见到浅蓝色火焰
- B.H2为正极,O2为负极
- C.工作时电解液的OH—的物质的量不断增加
- D.电极反应为:负极H2失电子;正极 O2得电子
D
试题分析:原电池中负极失去电子,发生氧化反应。正极得到电子,发生还原反应,所以氢气在负极通入,氧气在正极通入。因此选项D正确,B不正确;A不正确,不可能产生浅蓝色火焰,C不正确,根据总反应式可知,OH-的物质的量是不变的,答案选D。
考点:考查原电池的有关判断
点评:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应,据此可以进行有关的判断和计算。
试题分析:原电池中负极失去电子,发生氧化反应。正极得到电子,发生还原反应,所以氢气在负极通入,氧气在正极通入。因此选项D正确,B不正确;A不正确,不可能产生浅蓝色火焰,C不正确,根据总反应式可知,OH-的物质的量是不变的,答案选D。
考点:考查原电池的有关判断
点评:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应,据此可以进行有关的判断和计算。

练习册系列答案
相关题目

 美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如图所示:a、b两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电.
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如图所示:a、b两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电.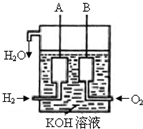 已知在25°C、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:
已知在25°C、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题: (1)已知:TiO2(s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ?mol-1;
(1)已知:TiO2(s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ?mol-1; 氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol
氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol