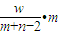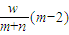题目内容
X元素的离子X2-,核外电子数为m,中子数为n,wg X的氢化物中的电子为( )mol.
A.
| B.
| C.
| D.
|
X2-核外电子数为m、核内中子数为n,则X的核外电子数为(m-2),核内中子数也为n,质子数同电子数(m-2).则X的质量数=质子数+中子数=(m-2+n),其氢化物为XH2,其相对分子质量M=m-2+n+2=m+n
则wg XH2的物质的量为
=
mol
而每个分子有电子数为m-2+2=m
那么wg XH2中含有电子的物质的量为
×m=
故选A.
则wg XH2的物质的量为
| w |
| M |
| W |
| m+n |
而每个分子有电子数为m-2+2=m
那么wg XH2中含有电子的物质的量为
| w |
| M |
| wm |
| m+n |
故选A.

练习册系列答案
相关题目
某主族元素的离子X2+有6个电子层,最外层有2个电子,当把XO2溶于浓盐酸时,有黄色气体产生,则下列说法不正确的是
| A.X2+具有还原性 | B.X的+2价化合物比+4价化合物稳定 |
| C.XO2具有强氧化性 | D.该元素是第ⅡA族元素 |