题目内容
某二元酸(简写为H2A)溶液,按下式发生电离:H2A![]() H++HA- HA-
H++HA- HA-![]() H++A2-,已知NaHA的溶液呈碱性.
H++A2-,已知NaHA的溶液呈碱性.
设有下列四种溶液:
A.0.01 mol·L-1的H2A溶液
B.0.01 mol·L-1的NaHA溶液
C.0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液
D.0.02 mol·L-1的NaOH与0.02 mol·L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号):
(1)c(H+)最大的是________,最小的是________.
(2)c(H2A)最大的是________,最小的是________.
(3)c(A2-)最大的是________,最小的是________.
答案:(1)A,D;(2)C,D;(3)D,A
解析:
解析:
|
从电离方程式可知该二元酸为二元弱酸,且HA-的水解程度大于其电离程度.c(H+)最大的是溶液酸性最强A,因B选项中溶质为酸式盐,电离出H+程度比酸小;C选项中溶质反应完后为0.01 mol·L-1的H2A与0.01 mol·L-1的NaHA的混合溶液,HA-离子会抑制H2A的电离,产生的H+会减少.D选项中溶质反应完后正盐,只有水解没有电离应该是碱性溶液,c(H+)浓度最小.同理:c(H2A)最大的为C,最小的为D.c(A2-)最大的是D因该溶液中溶质为正盐,最小的是A,因其溶液的酸性最强,c(A2-)最小. |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
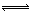 H++A2- ,已知常温下浓度为0.1mol/L的H2A溶液中c(H+)=0.11mol/L,则关于0.1mol/L的NaHA溶液的下列叙述中正确的是:( )
H++A2- ,已知常温下浓度为0.1mol/L的H2A溶液中c(H+)=0.11mol/L,则关于0.1mol/L的NaHA溶液的下列叙述中正确的是:( )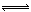 H++A2-,已知常温下浓度为0.1mol/L的H2A溶液中c(H+)=0.11mol/L,则关于0.1mol/L的NaHA溶液的下列叙述中正确的是:( )
H++A2-,已知常温下浓度为0.1mol/L的H2A溶液中c(H+)=0.11mol/L,则关于0.1mol/L的NaHA溶液的下列叙述中正确的是:( )