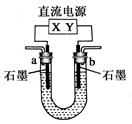
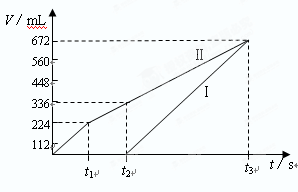
题目内容
下列说法正确的是
| A.原电池反应是自发的氧化还原反应,盐桥的作用是平衡正负极电荷, 形成闭合回路 |
| B.为防止轮船发生腐蚀,往往在轮船外壳焊上金属锌,这是牺牲阴极的阳极保护法 |
| C.精炼铜时,粗铜做阳极,纯铜做阴极,CuSO4是电解质溶液,电解前后溶液浓度不变 |
| D.电镀是特殊的电解,电解前后阴极减少的质量与阳极增加的质量相等 |
A
试题分析:B、为防止轮船发生腐蚀,往往在轮船外壳焊上金属锌,锌活泼,这是牺牲阳极的阴极保护法,B错;C、精炼铜时,粗铜做阳极,纯铜做阴极,CuSO4是电解质溶液,电解前后CuSO4溶液浓度减小,粗铜放电时,,比铜活泼的金属优先放电,而溶液中的铜离子放电,所以电解前后溶液浓度减小;D、电镀是特殊的电解,,阳极材料本身放电,所以电解前后阳极减少的质量与阴极增加的质量相等,D错。故选AS。
点评:熟练掌握电解的相关知识,尤其是电解池和电镀池,电解质溶液的变化区别,前者变小,后者基本不变

练习册系列答案
相关题目