题目内容
可以说明反应2HI(g)![]() H2(g)+I2(g)已达到平衡的是( )
H2(g)+I2(g)已达到平衡的是( )
① 单位时间内生成n mol H2的同时生成n mol HI
② 一个H-H键断裂的同时有两个H-I键断裂
③ 百分组成ω(HI)=ω(I2)
④ 反应速率υ(H2)=υ(I2)=1/2υ(HI)时
⑤ c(HI):c(H2):c(I2)=2:1:1时
⑥ 温度和体积一定时,容器内压强不再变化
⑦ 温度和体积一定时,某一生成物浓度不再变化
⑧ 条件一定,混合气体的平均相对分子质量不再变化
⑨ 温度和体积一定时,混合气体的颜色不再变化
⑩ 温度和压强一定时,混合气体的密度不再变化
A.②③⑤ B.①④⑦ C.②⑦⑨ D⑧⑨⑩
C
解析:略

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
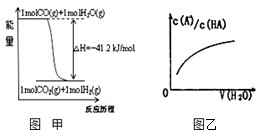 关于下列各图的叙述错误的是( )
关于下列各图的叙述错误的是( )| 化学方程式 | 平衡常数K |
| F2+H2?2HF | 6.5×1095 |
| Cl2+H2?2HCl | 2.6×1033 |
| Br2+H2?2HBr | 1.9×1019 |
| I2+H2?2HI | 8.7×102 |
| A、已知1molCO燃烧放出的热为283kJ,2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol则图甲表示CO和H2O(g)生成CO2和H2的能量变化 | ||
| B、常温下0.4 mol?L-1 HB溶液和0.2 mol?L-1NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(B-)>c(Na+)>c(H+)>c(OH-) | ||
| C、常温下,X2(g)和H2反应生成HX的平衡常数如表所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐减小,且HX的还原性逐渐减弱 | ||
D、图乙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
|
 H2(g)+I2(g)已达平衡状态的是
H2(g)+I2(g)已达平衡状态的是  H2(g)+I2(g)已达到平衡的是( )
H2(g)+I2(g)已达到平衡的是( ) H2(g)+I2(g)已达到平衡的是( )
H2(g)+I2(g)已达到平衡的是( )