题目内容
14.下列有关有机化合物的说法正确的是( )| A. | 聚乙烯可以使溴水褪色 | |
| B. | 乙烷与氯气发生取代反应,产物共有7种 | |
| C. | 煤中含有苯、甲苯和二甲苯 | |
| D. | 乙酸和油脂都能与NaOH溶液反应 |
分析 A.聚乙烯中不含碳碳双键;
B.乙烷与氯气发生取代反应能够生成一元取代、二元取代…到完全取代,注意多元取代时,可以确定相同碳原子上的氢原子,也可以确定不同碳原子上的氢原子,发生n元取代与m元取代,若n+m等于氢原子数目,则取代产物种数相同;
C.煤的干馏产物含芳香烃;
D.乙酸含-COOH,油脂含-COOC-.
解答 解:A.聚乙烯中不含碳碳双键,不能使溴水褪色,故A错误;
B.乙烷中所有氢原子都等效,则其一氯取代物只有1种,二氯取代物有2种,三氯取代物有2种,四氯取代物有2种(与二溴取代物个数相同),五氯取代物有1种(与一溴取代物个数相同),六氯取代物1种,所以共有9种,故B错误;
C.煤的干馏产物中含有苯、甲苯和二甲苯,而煤中不含,故C错误;
D.乙酸含-COOH,油脂含-COOC-,分别与NaOH发生中和反应、水解反应,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意同分异构体的判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.水晶是重要的首饰用品,其主要成分是SiO2,下列有关SiO2的说法正确的是( )
| A. | 水晶能溶于水生成H2SiO3 | |
| B. | SiO2是酸性氧化物,不能与任何酸反应 | |
| C. | SiO2既能溶于NaOH溶液,又能溶于HF,因此属于两性氧化物 | |
| D. | SiO2对应的H2SiO3是一种弱酸,酸性比碳酸还弱 |
2.下列关于著名科学家及其成就的描叙不正确的是( )
| A. | 德国化学家维勒第一次人工合成了尿素,从而揭开了人工合成有机物的序幕 | |
| B. | 中国化学家侯德榜成功发明了侯氏制碱法,打破了外国当时对中国的相关技术封锁 | |
| C. | 英国科学家卢瑟福根据α粒子散射实验提出了“葡萄干面包式”原子结构模型 | |
| D. | 俄国化学家门捷列夫在前人基础上研究提出了元素周期律并列出了第一张元素周期表 |
9.下列离子方程式不正确的是( )
| A. | 用Cu作阳极电解饱和食盐水:Cu+2H+$\frac{\underline{\;电解\;}}{\;}$Cu2++H2↑ | |
| B. | Fe3O4溶于氢碘酸溶液中:Fe3O4+8H++2I-=3Fe2++I2+4H2O | |
| C. | NH4Al(SO4)2溶于过量的浓Ba(OH)2溶液中:NH4++A13++2SO42-+2Ba2++5OH-=2BaSO4↓+AlO2-+NH3↑+H2O | |
| D. | 澄清石灰水中充入过量的SO2:SO2+OH-=HSO3- |
19.已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法:
I.还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬.具体流程如下:
Cr2O${\;}_{7}^{2-}$$→_{适量FeSO_{4}溶液}^{①H_{2}SO_{4}溶液}$Cr3+$\stackrel{③调节pH}{→}$Cr(OH)3$\stackrel{③加热}{→}$Cr2O3
有关离子完全沉淀的pH如表:
(1)写出Cr2O72-与FeSO4溶液在酸性条件下反应的离子方程式Cr2O72-+6Fe2++14H+═2 Cr3++6Fe3++7H2O.
(2)还原+6价铬还可选用以下的BD试剂(填序号).
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.
则在操作②中可用于调节溶液pH的试剂为:CD(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在B(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
II.电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(4)写出阴极的电极反应式2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-.
(5)电解法中加入氯化钠的作用是:氯化钠是强电解质,增强溶液导电性.
I.还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬.具体流程如下:
Cr2O${\;}_{7}^{2-}$$→_{适量FeSO_{4}溶液}^{①H_{2}SO_{4}溶液}$Cr3+$\stackrel{③调节pH}{→}$Cr(OH)3$\stackrel{③加热}{→}$Cr2O3
有关离子完全沉淀的pH如表:
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(2)还原+6价铬还可选用以下的BD试剂(填序号).
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.
则在操作②中可用于调节溶液pH的试剂为:CD(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在B(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
II.电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去.
(4)写出阴极的电极反应式2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-.
(5)电解法中加入氯化钠的作用是:氯化钠是强电解质,增强溶液导电性.
6.四种短周期元素W、X、Y、Z,其原子的最外层电子数之和为19,W和X元素原子核的质子数之比为1:2,Y的核外电子数比X多4,Z的核电荷数大于X.下列说法正确的是( )
| A. | 原子半径大小:Z>Y>X>W | |
| B. | 由W元素形成的单质一定是原子晶体,其熔沸点很高 | |
| C. | W、Y、Z三种元素形成的气态氢化物中最稳定的是Z的气态氢化物 | |
| D. | Y、Z所形成的氧化物的水化物的酸性为:Y<Z |
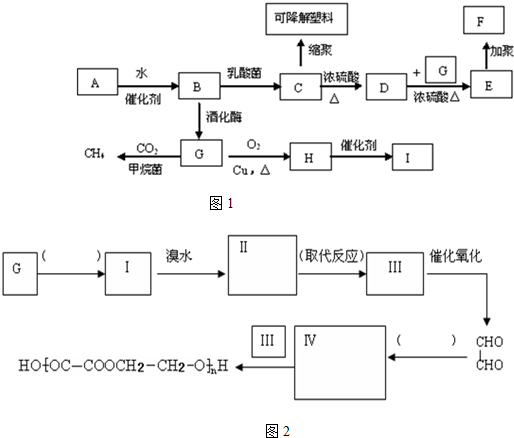
 六元环状化合物I
六元环状化合物I
 .
. 的合成路线如图2:(按要求填写,消去反应;氧化反应内填写反应类型,内填写Ⅱ和Ⅳ的结构简式)
的合成路线如图2:(按要求填写,消去反应;氧化反应内填写反应类型,内填写Ⅱ和Ⅳ的结构简式)