题目内容
2.如果铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为0.012mg.那么一个铅笔字含有的碳原子数约为3.01×1017个(用数字表示)分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$计算.
解答 解:n(C)=$\frac{1}{2}$×$\frac{0.012mg×1{0}^{-3}\frac{g}{mg}}{12g/mol}$=0.5×10-6mol,N(C)=0.5×10-6mol×6.02×1023/mol=3.01×1017,
故答案为:3.01×1017.
点评 本题考查物质中原子数目及常用化学计量计算,为高频考点,侧重于学生的分析能力和计算能力的考查,比较基础,注意公式的灵活运用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.某烃的结构简式为 ,它可能具有的性质是( )
,它可能具有的性质是( )
 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 易溶于水,也易溶于有机溶剂 | |
| B. | 1 mol该烃含有4 mol碳碳双键 | |
| C. | 能发生聚合反应,其产物可表示为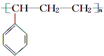 | |
| D. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 |
13.下列比较不正确的是( )
| A. | 非金属性:C>N | B. | 酸性:HClO4>H2CO3 | ||
| C. | 碱性:NaOH>Mg(OH)2 | D. | 热稳定性H2O>H2S |
10.下列食物中属于酸性食物的是( )
| A. | 西红柿 | B. | 羊肉 | C. | 柠檬 | D. | 黄瓜 |
7.下列溶液中有关微粒的物质的量浓度关系错误的是( )
| A. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(NH4+)+c(OH-)>c(Cl-)+c(H+) | |
| B. | 等体积、等物质的量浓度为Na2CO3溶液与NaHCO3溶液混合后:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) | |
| C. | 浓度相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液中,c(NH4+)大小顺序为:②>③>① | |
| D. | 0.1 mol/L Na2CO3溶液与0.1 mol/L HCl溶液等体积混合,所得溶液中:c(H+)+c(H2CO3)=c(CO32-)+c(OH-) |
11.下列说法正确的是( )
①可用酒精萃取碘水中的碘单质;
②用酒精灯加热试管内固体时,一定要先给试管预热再集中对准药品加热;
③分离碘的CCl4溶液应使用蒸馏法;
④用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部;
⑤稀释浓硫酸时,把水慢慢倒入盛有浓硫酸的烧杯中;
⑥配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出;
⑦检测某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸.
①可用酒精萃取碘水中的碘单质;
②用酒精灯加热试管内固体时,一定要先给试管预热再集中对准药品加热;
③分离碘的CCl4溶液应使用蒸馏法;
④用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部;
⑤稀释浓硫酸时,把水慢慢倒入盛有浓硫酸的烧杯中;
⑥配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出;
⑦检测某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸.
| A. | ①②④⑤⑦ | B. | ①②③④⑥ | C. | ①④⑦⑥ | D. | ②③④ |
4.在容积为2L的密闭容器中进行反应,CO(g)+2H2(g)?CH3OH(g),其他条件不变,在300℃和500℃时,n(CH3OH)与反应时间t的变化曲线如图,下列说法正确的是( )


| A. | 该反应的△H<0 | |
| B. | 其他条件不变,升高温度反应的平衡常数增大 | |
| C. | 300℃时,0~t1min内CH3OH的平均生成速率为$\frac{{n}_{1}}{{t}_{1}}$1mol•L-1•min-1 | |
| D. | A点的反应体系温度从300℃升高到500℃,达到平衡时,$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$减小 |
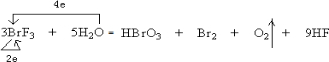 ,还原剂是H2O和BrF3,氧化剂是BrF3.氧化产物是HBrO3、O2. 还原产物是Br2(以上均填化学式)
,还原剂是H2O和BrF3,氧化剂是BrF3.氧化产物是HBrO3、O2. 还原产物是Br2(以上均填化学式)