题目内容
用惰性电极电解1 L 0.1 mol·L-1含Cu2+、X3+的水溶液,阴极质量的增重与通过电子的物质的量关系如图4-15所示,则溶液中离子的氧化性由强到弱的顺序是(X3+无可变价态)
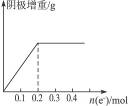
图4-15 通过电子的物质的量
- A.Cu2+>X3+>H+
- B.X3+>Cu2+>H+
- C.Cu2+>H+>X3+
- D.H+>Cu2+>X3+
C
阴极增重只能是析出的Cu或X或X+Cu的质量,由通过0.2 mol e-后阴极质量不再增加可知仅析出了Cu,而没有析出X。
阴极增重只能是析出的Cu或X或X+Cu的质量,由通过0.2 mol e-后阴极质量不再增加可知仅析出了Cu,而没有析出X。

练习册系列答案
相关题目
NA为阿伏加德罗常数,下列叙述正确的是
A.0.5mol雄黄(As4S4,已知As和N同主族,结构如右图)含有NA个S—S键 |
| B.用惰性电极电解1 L浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 NA个电子转移时,阴极析出6.4g金属 |
| C.1mol过氧化氢分子中共用电子对数为3NA |
| D.0.1mol Na2CO3·10H2O在晶体中或溶液中,含有的CO32-离子均小于0.1 NA |