题目内容
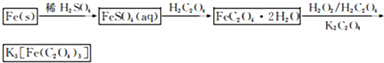
写出下列制备法中的化学方程式:
(1)实验室以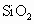 、NaOH溶液、盐酸为主要原料,制备少量原硅酸
、NaOH溶液、盐酸为主要原料,制备少量原硅酸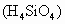 :
:
________________________________________________________________________________
(2)工业上以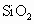 、焦炭、
、焦炭、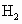 、
、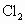 为主要原料制备单晶硅:
为主要原料制备单晶硅:
________________________________________________________________________________
________________________________________________________________________________
答案:
解析:
解析:
|
(1) (2) |

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
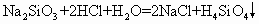

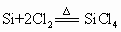
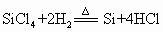
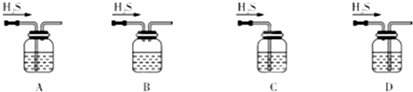
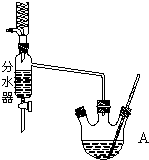 如图为制取乙酸乙酯的实验装置图.回答下列问题:
如图为制取乙酸乙酯的实验装置图.回答下列问题: