题目内容
已知:将Cl2通人适量KOH溶液,产物中可能有KC1、KClO、KC1O3,且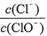 的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是
的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是
A.若某温度下,反应后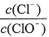 =11,则溶液中
=11,则溶液中 =
=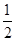
参加反应的氯气的物质的量等于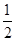 amol
amol
C.改变温度,反应中转移电子的物质的量ne的范围: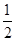 amol≤ne≤
amol≤ne≤ amol
amol
D.改变温度,产物中KC1O3的最大理论产量为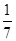 amol
amol
D
解析试题分析:A项若反应后 =11,令KC1、KClO分别为11 mol、1 mol,据得失电子守恒可得KC1O3为2 mol,则溶液中
=11,令KC1、KClO分别为11 mol、1 mol,据得失电子守恒可得KC1O3为2 mol,则溶液中 =
= ,正确;B项据原子守恒n(KOH)=amol=n(K) =n(Cl) =2n(Cl2),则n(Cl2) =
,正确;B项据原子守恒n(KOH)=amol=n(K) =n(Cl) =2n(Cl2),则n(Cl2) = amol,正确;C项采用极限法分析,当全部生成KC1、KClO时发生的反应为Cl2+2KOH=KCl+KClO+H2O,则ne=
amol,正确;C项采用极限法分析,当全部生成KC1、KClO时发生的反应为Cl2+2KOH=KCl+KClO+H2O,则ne= amol,同理,当全部生成KC1、KClO3时发生的反应为3Cl2+6KOH=5KCl+KClO3+3H2O,则ne=
amol,同理,当全部生成KC1、KClO3时发生的反应为3Cl2+6KOH=5KCl+KClO3+3H2O,则ne= amol,综上可得改变温度,反应中转移电子的物质的量ne的范围:
amol,综上可得改变温度,反应中转移电子的物质的量ne的范围: amol≤ne≤
amol≤ne≤ amol,该项正确;D项改变温度,产物中KC1O3的最大理论产量即无KClO生成,发生如下反应:3Cl2+6KOH=5KCl+KClO3+3H2O,则KC1O3的物质的量为
amol,该项正确;D项改变温度,产物中KC1O3的最大理论产量即无KClO生成,发生如下反应:3Cl2+6KOH=5KCl+KClO3+3H2O,则KC1O3的物质的量为 amol,故该项错误。
amol,故该项错误。
考点:考查氧化还原反应的相关计算(涉及极限法、原子守恒法等)。

常温下,在水溶液中发生如下反应:( )
①16H++10C-+2XO4 - = 2X2++5C2+8H2O;②2A2++B2 = 2A3++2B-;③2B-+C2 = B2+2C-。
下列说法错误的是
| A.反应C2 + 2A2+ = 2A3+ + 2C- 可以进行 |
| B.还原性由强到弱的顺序是C->A2+>B->X2+ |
| C.氧化性由强到弱的顺序是XO4->C2>B2>A3+ |
| D.反应③是置换反应 |
在真空密闭装置中,亚氯酸钠(NaClO2)固体在一定条件下发生分解反应,从物质组成的角度看,不可能生成的产物是
| A.NaCl和O2 | B.NaClO3和NaClO |
| C.NaClO3和Cl2 | D.NaClO3和NaCl |
今有下列三个氧化还原反应:
①2FeCl3+2KI===2FeCl2+2KCl+I2
②2FeCl2+Cl2===2FeCl3
③2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O
若某溶液中有Fe2+、I-、Cl-共存,要除去I-而不氧化Fe2+和Cl-,则可加入的试剂是
| A.Cl2 | B.KMnO4 | C.HCl | D.FeCl3 |
给汽车安装尾气净化装置,汽车尾气通过净化装置(内有钯等过渡金属元素做催化剂)后,其中的有害气体CO、NO转化为无害气体N2、CO2则( )
| | A. | NO作为还原剂 | B. | CO作为还原剂 | C. | N2作为还原剂 | D. | CO2作为氧化剂 |
实验室将NaClO3和Na2SO3按物质的量为2:1放入烧杯中,同时滴入适量H2SO4,并用水浴加热,产生棕黄色的气体X,反应后测得NaClO3和Na2SO3恰好完全反应,则X的化学式为
| A.Cl2 | B.Cl2O | C.ClO2 | D.Cl2O3 |
X、Y代表两种非金属元素,下列不能说明非金属性X比Y强的是( )。
| A.Y的阴离子Y 2-的还原性强于X的阴离子X- |
| B.X的含氧酸的酸性比Y的含氧酸的酸性强 |
| C.X的单质X2能将Y的阴离子Y 2-氧化,并发生置换反应 |
| D.X的氢化物比Y的氢化物稳定 |
下列反应中,H2O作还原剂的是
| A.2Na2O2+2H2O =" 4NaOH" + O2↑ | B.2F2+2H2O =" 4HF" + O2↑ |
| C.3NO2 + H2O =" NO" + 2HNO3 | D.3Fe+4H2O(g) 4H2+Fe3O4 4H2+Fe3O4 |
火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2→Cu2S+2FeS+SO2下列说法正确的是
| A.SO2只是氧化产物 |
| B.CuFeS2仅作还原剂,硫元素被氧化 |
| C.每生成1molCu2S,有4mol硫被氧化 |
| D.每转移1.2mol电子,有0.2mol硫被氧化 |