题目内容
18.已知A的产量通常用来衡量一个国家的石油化工发展水平,B、D是饮食中两种常见的有机物,F是一种有香味的物质,F中碳原子数是D的两倍.现以A为主要原料合成F和高分子化合物E,其合成路线如图1所示.(1)写出A的电子式:
 .
.(2)写出D中官能团的名称:羧基.
(3)写出E的结构简式:
 .
.(4)写出①的化学方程式:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(5)物质B可以直接氧化为物质D,需要加入的试剂是高锰酸钾或重铬酸钾.
(6)苯是石油化工的重要产品,在浓硫酸的作用下,苯在50℃~60℃与浓硝酸发生反应,写出反应化学方程式
 .
.(7)在实验室里我们可以用如图2所示的装置来制取F,乙中所盛的试剂为饱和碳酸钠溶液,甲中发生的化学方程式为:CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O;该装置图中有一个明显的错误是乙中导管在液面下.

分析 A的产量通常用来衡量一个国家石油化工水平,则A是CH2=CH2,乙烯和水发生加成反应生成B为CH3CH2OH,乙醇发生氧化反应生成C为CH3CHO,F是一种有香味的物质,D是生活中常见的有机物,F中碳原子数是D的两倍,可知D为CH3COOH,乙酸与乙醇发生酯化反应生成F为CH3COOCH2CH3,乙烯发生加聚反应生成高分子化合物E为 ,以此来解答.
,以此来解答.
解答 解:(1)A是CH2=CH2,结构式为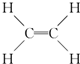 ,其电子式为
,其电子式为 ,故答案为:
,故答案为: ;
;
(2)D为CH3COOH,官能团的名称为羧基,故答案为:羧基;
(3)E的结构简式为 ,故答案为:
,故答案为: ;
;
(4)①的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(5)物质B可以直接氧化为物质D,需要加入的试剂是高锰酸钾或重铬酸钾等,故答案为:高锰酸钾或重铬酸钾;
(6)在浓硫酸的作用下,苯在50℃~60℃与浓硝酸发生取代反应生成硝基苯,反应化学方程式为 ,
,
故答案为: ;
;
(7)由图可知,乙中所盛的试剂为饱和碳酸钠溶液,甲中发生的化学方程式为CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O;该装置图中有一个明显的错误是乙中导管在液面下,可发生倒吸,故答案为:饱和碳酸钠溶液;CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O;乙中导管在液面下.
点评 本题考查有机物的推断,为高频考点,把握A为乙烯、流程中碳原子数变化、有机反应为解答的关键,侧重分析与推断能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.如图为原电池示意图,下列说法正确的是( )


| A. | 该装置能够将化学能转化成电能 | B. | 锌是负极,发生还原反应 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 铜是负极,发生氧化反应 |
13.下列有关化学用语正确的是( )
| A. | HCl的电子式为: | B. | Cl-的结构示意图为: | ||
| C. | CO2的电子式: | D. | 乙烯的结构简式是CH2CH2 |
10.在K2CO3样品中含Na2CO3、KNO3、Ba(NO3)2中的一或两种杂质.将13.8g该样品溶于足量水中得到澄清溶液,再加入过量CaCl2溶液,可得9.0g沉淀,则原样品中含有的杂质会是( )
| A. | 肯定含有KNO3,没有Ba(NO3)2;可能含有Na2CO3 | |
| B. | 肯定含有Na2CO3,没有Ba(NO3)2 | |
| C. | 肯定没有Na2CO3,Ba(NO3)2 | |
| D. | 无法判断含何种杂质 |
7.4-溴甲基-1-环己烯的一种合成路线如图:

下列说法正确的是( )

下列说法正确的是( )
| A. | ①是加成反应,②是还原反应 | |
| B. | W存在顺反异构,另一种结构为 | |
| C. | X的官能团由烯键和酯基 | |
| D. | 按照系统命名法, 为乙烯基丙酸乙酯 为乙烯基丙酸乙酯 |
6. 用AG表示溶液酸度:AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.在室温下,用0.1mol/L的HCl溶液滴定20.00mL0.1mol/L氨水.滴定结果可表示如图:下列分析正确的是( )
用AG表示溶液酸度:AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.在室温下,用0.1mol/L的HCl溶液滴定20.00mL0.1mol/L氨水.滴定结果可表示如图:下列分析正确的是( )
 用AG表示溶液酸度:AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.在室温下,用0.1mol/L的HCl溶液滴定20.00mL0.1mol/L氨水.滴定结果可表示如图:下列分析正确的是( )
用AG表示溶液酸度:AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.在室温下,用0.1mol/L的HCl溶液滴定20.00mL0.1mol/L氨水.滴定结果可表示如图:下列分析正确的是( )| A. | 0.lmol/L 氨水 pH=10.2 | |
| B. | A点加入盐酸的体积为20.00mL | |
| C. | 若a=7,从A到B水的电离程度逐渐减小 | |
| D. | B点溶液中可能存在c(Cl-)>c(NH4+)>(H+)>c(OH-) |




