题目内容
硝酸钾是一种重要的化工产品,工业上制备硝酸钾的流程如图所示:
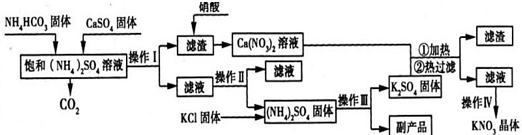
请回答下列问题:
(1)在饱和(NH4)2SO4溶液中,CaSO4与NH4HCO3按物质的量之比1:2恰好完全反应,该反应的化学方程式为
(2)操作Ⅰ是
(3)操作Ⅲ的化学方程式是
(4)Ca(NO3)2溶液和K2SO4固体反应后需要热过滤的原因是
(5)本实验中可以循环利用的物质是

请回答下列问题:
(1)在饱和(NH4)2SO4溶液中,CaSO4与NH4HCO3按物质的量之比1:2恰好完全反应,该反应的化学方程式为
CaSO4+2NH4HCO3=CaCO3↓+(NH4)2SO4+H2O+CO2↑
CaSO4+2NH4HCO3=CaCO3↓+(NH4)2SO4+H2O+CO2↑
(2)操作Ⅰ是
过滤、蒸发浓缩
过滤、蒸发浓缩
,操作Ⅱ是冷却结晶
冷却结晶
,操作Ⅲ是过滤、加热冷却结晶
过滤、加热冷却结晶
,操作Ⅳ是过滤
过滤
.(3)操作Ⅲ的化学方程式是
(NH4)2SO4+2KCl
K2SO4+2NH3↑+2HCl↑
| ||
(NH4)2SO4+2KCl
K2SO4+2NH3↑+2HCl↑
,该反应中得到的副产物是
| ||
NH4Cl
NH4Cl
.(4)Ca(NO3)2溶液和K2SO4固体反应后需要热过滤的原因是
防止KNO3冷却时结晶析出,从而导致产率下降
防止KNO3冷却时结晶析出,从而导致产率下降
.(5)本实验中可以循环利用的物质是
硫酸钙
硫酸钙
(写名称).分析:分析整个流程图知,操作Ⅰ是将滤渣与滤液分开,应是过滤操作,向滤液中加入硝酸生成Ca(NO3)2,可知滤渣是碳酸钙沉淀,而滤液中未加入任何物质,精操作Ⅱ又得滤液和(NH4)2SO4固体,由此可知原滤液就是硫酸铵溶液,据此可以推出第一步反应的化学方程式,同时可知操作Ⅱ是将硫酸铵从溶液中结晶出来;通过操作Ⅲ使两种固体直接反应,显然操作Ⅲ是加热;最后一步发生复分解反应制的硝酸钾.
解答:解:(1)在饱和(NH4)2SO4溶液中,CaSO4与NH4HCO3按物质的量之比1:2恰好完全反应,该反应的化学方程式为:CaSO4+2NH4HCO3=CaCO3↓+(NH4)2SO4+H2O+CO2↑,
故答案为:CaSO4+2NH4HCO3=CaCO3↓+(NH4)2SO4+H2O+CO2↑;
(2)分析整个流程图知,操作Ⅰ是将滤渣与滤液分开,应是过滤操作,向滤液中加入硝酸生成Ca(NO3)2,可知滤渣是碳酸钙沉淀,而滤液中未加入任何物质,精操作Ⅱ又得滤液和(NH4)2SO4固体,由此可知原滤液就是硫酸铵溶液,据此可以推出第一步反应的化学方程式,同时可知操作Ⅱ是将硫酸铵从溶液中结晶出来;通过操作Ⅲ使两种固体直接反应,显然操作Ⅲ是加热;最后一步发生复分解反应制的硝酸钾,操作Ⅳ是过滤,
故答案为:过滤、蒸发浓缩;冷却结晶;过滤、加热冷却结晶;过滤;
(3)操作Ⅲ是硫酸铵和氯化钾加热反应生成硫酸钾,氯化氢和氨气,反应的化学方程式是:(NH4)2SO4+2KCl
K2SO4+2NH3↑+2HCl↑,氯化氢和氨气冷却结合生成氯化铵副产物,
故答案为:(NH4)2SO4+2KCl
K2SO4+2NH3↑+2HCl↑;NH4Cl;
(4)Ca(NO3)2溶液和K2SO4固体反应后需要热过滤的原因是,防止KNO3冷却时结晶析出,从而导致产率下降,
故答案为:防止KNO3冷却时结晶析出,从而导致产率下降;
(5)依据流程图和反应过程分析可知循环利用的物质时参与反应过程,最后又生成的物质,结合反应过程分析,硫酸钙是可循环利用的物质,故答案为:硫酸钙.
故答案为:CaSO4+2NH4HCO3=CaCO3↓+(NH4)2SO4+H2O+CO2↑;
(2)分析整个流程图知,操作Ⅰ是将滤渣与滤液分开,应是过滤操作,向滤液中加入硝酸生成Ca(NO3)2,可知滤渣是碳酸钙沉淀,而滤液中未加入任何物质,精操作Ⅱ又得滤液和(NH4)2SO4固体,由此可知原滤液就是硫酸铵溶液,据此可以推出第一步反应的化学方程式,同时可知操作Ⅱ是将硫酸铵从溶液中结晶出来;通过操作Ⅲ使两种固体直接反应,显然操作Ⅲ是加热;最后一步发生复分解反应制的硝酸钾,操作Ⅳ是过滤,
故答案为:过滤、蒸发浓缩;冷却结晶;过滤、加热冷却结晶;过滤;
(3)操作Ⅲ是硫酸铵和氯化钾加热反应生成硫酸钾,氯化氢和氨气,反应的化学方程式是:(NH4)2SO4+2KCl
| ||
故答案为:(NH4)2SO4+2KCl
| ||
(4)Ca(NO3)2溶液和K2SO4固体反应后需要热过滤的原因是,防止KNO3冷却时结晶析出,从而导致产率下降,
故答案为:防止KNO3冷却时结晶析出,从而导致产率下降;
(5)依据流程图和反应过程分析可知循环利用的物质时参与反应过程,最后又生成的物质,结合反应过程分析,硫酸钙是可循环利用的物质,故答案为:硫酸钙.
点评:本题考查了物质制备流程分析判断,实验操作步骤的分析理解,物质性质的分析应用,主要是物质分离实验基本操作的应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
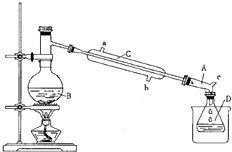 溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的反应和实验装置如下:
溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的反应和实验装置如下:反应:CH3CH2OH+BHr
| 浓H2SO4 |
装置如图.
实验中可能用到的数据如表:
| 物质 | 相对分子质量 | 沸点/℃ | 密度/g?cm-3 | 水溶性 |
| CH3CH2OH | 46 | 78.4 | 0.79 | 互溶 |
| CH3CH2Br | 109 | 38.4 | 1.42 | 难溶 |
| CH3CH2OCH2CH3 | 74 | 34.5 | 0.71 | 微溶 |
| CH2=CH2 | 28 | -103.7 | 0.38 | 不溶 |
| 浓硫酸(H2SO4) | 98 | 338 | 1.38 | 易溶 |
②分离提纯:将馏出物加水后振荡,再加入适量酸除去乙醚,分液,最后得到52mL溴乙烷.
回答下列问题:
(1)仪器B的名称是
(2)仪器C为直形冷凝管,冷水进口是
(3)仪器D置于盛有
(4)装置A的名称为牛角管,其结构中的c支管的作用是
(5)溴乙烷粗产品分离提纯阶段,加水的目的是
(6)该实验所得溴乙烷的产率为

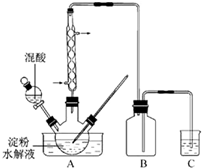 (2011?江苏)草酸是一种重要的化工产品.实验室用硝酸氧化淀粉水解液制备草酸的装置如图14所示(加热、搅拌和仪器固定装置均已略去)
(2011?江苏)草酸是一种重要的化工产品.实验室用硝酸氧化淀粉水解液制备草酸的装置如图14所示(加热、搅拌和仪器固定装置均已略去)