题目内容
将一定量的NO2充入量筒中并倒立于水槽中,待量筒中的液面不再上升时,向量筒中缓缓通入O2.当耗掉O2 42mL时量筒中的液面与未通O2前等高,则NO2的体积为( )
分析:二氧化氮和水反应的方程式为:3NO2+H2O=2HNO3+NO,一氧化氮和氧气反应生成二氧化氮,二氧化氮又和水反应生成硝酸和一氧化氮,当充入的氧气少量时,剩余的气体是一氧化氮,液面上升,NO与通入的氧气恰好反应时,溶液充满整个试管,当充入的氧气过量时,液面下降,若要使试管内液面仍保持在原高度,剩余的气体是氧气,等于原来生成NO的体积.
解答:解:二氧化氮和水反应的方程式为:3NO2+H2O=2HNO3+NO,一氧化氮和氧气反应生成二氧化氮,二氧化氮又和水反应生成硝酸和一氧化氮,当充入的氧气少量时,剩余的气体是一氧化氮,液面上升,NO与通入的氧气恰好反应时,溶液充满整个试管,当充入的氧气过量时,液面下降,若要使试管内液面仍保持在原高度,剩余的气体是氧气,等于原来生成NO的体积,
设原来二氧化氮的体积为V,根据3NO2+H2O=2HNO3+NO知,生成一氧化氮的体积为二氧化氮体积的
,则最后剩余氧气的体积为
,根据4NO+3O2+2H2O=4HNO3知,一氧化氮完全反应需要氧气体积=
=
,反应的氧气和未反应的氧气体积之和为42mL,即
+
=42mL,V=72mL,
故选C.
设原来二氧化氮的体积为V,根据3NO2+H2O=2HNO3+NO知,生成一氧化氮的体积为二氧化氮体积的
| V |
| 3 |
| V |
| 3 |
| ||
| 4 |
| V |
| 4 |
| V |
| 3 |
| V |
| 4 |
故选C.
点评:本题考查氮的氧化物性质、根据方程式计算的计算等,清楚发生的反应是解题关键,注意利用总反应方程式进行的解答,难度中等.

练习册系列答案
相关题目
A是由导热材料制成的钢化密闭容器,B是一耐化学腐蚀且易于传热的气球.关闭旋塞K.(已知:2NO2?N2O4;△H)
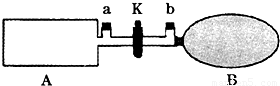
(1)若将一定量的NO2通过a充入A中,下表是该反应在不同温度下的化学平衡常数(K):
由表中数据判断△H 0(填“>”、“=”或“<”).
(2)若将等量的NO2通过a、b分别充入A、B中,反应起始时,A、B的体积相同.
一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是VA VB(填“>”、“<”、“=”);若打开旋塞K,气球B将 (填“变大”“变小”或“不变”).
(3)若在A、B中再充入与(2)中初始量相等的NO2,则达到平衡时,A中NO2的转化率将 (填“增大”“减小”或“不变”);若通入等量的Ne气,则达到平衡时,B中NO2的转化率将 (填“增大”“减小”或“不变”).
(4)室温下,若将等量的NO2通过a、b分别充入A、B中(关闭旋塞K),且A、B都保持体积不变,A套上一个绝热层,B与外界可以进行热传递,则达到平衡时, 中的颜色较深.

(1)若将一定量的NO2通过a充入A中,下表是该反应在不同温度下的化学平衡常数(K):
| 温度(K) | 273 | 308 | 373 |
| K-1 | 6.78 | 3.13 | 2.78 |
(2)若将等量的NO2通过a、b分别充入A、B中,反应起始时,A、B的体积相同.
一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是VA VB(填“>”、“<”、“=”);若打开旋塞K,气球B将 (填“变大”“变小”或“不变”).
(3)若在A、B中再充入与(2)中初始量相等的NO2,则达到平衡时,A中NO2的转化率将 (填“增大”“减小”或“不变”);若通入等量的Ne气,则达到平衡时,B中NO2的转化率将 (填“增大”“减小”或“不变”).
(4)室温下,若将等量的NO2通过a、b分别充入A、B中(关闭旋塞K),且A、B都保持体积不变,A套上一个绝热层,B与外界可以进行热传递,则达到平衡时, 中的颜色较深.


 NO + SO3 ,达到化学平衡时,下列叙述中正确的是
NO + SO3 ,达到化学平衡时,下列叙述中正确的是