题目内容
下列说法错误的是( )
| A、由于合成氨反应△H<0,△S>0,所以该反应能自发进行 | B、将pH=4的盐酸和醋酸稀释成pH=5的溶液,盐酸所需加入的水多 | C、溴水中有下列平衡:Br2+H2O?HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅 | D、弱电解质在溶液中达到电离平衡后,加水稀释,平衡向电离方向转移 |
分析:A、由于△H<0、△S<0,故合成氨反应能自发进行还和温度有关;
B、醋酸是弱电解质存在电离平衡,浓度大于盐酸,稀释到相同pH,醋酸加入的水多;
C、加入硝酸银,会和溴化氢反应生成溴化银浅黄色沉淀溴化银,促进平衡正向进行,溶液颜色变浅;
D、弱电解质存在电离平衡,加水稀释促进电离.
B、醋酸是弱电解质存在电离平衡,浓度大于盐酸,稀释到相同pH,醋酸加入的水多;
C、加入硝酸银,会和溴化氢反应生成溴化银浅黄色沉淀溴化银,促进平衡正向进行,溶液颜色变浅;
D、弱电解质存在电离平衡,加水稀释促进电离.
解答:解:A.N2(g)+3H2(g)═2NH3(g)△S<0,需在一定温度下才能进行,故A错误;
B、醋酸是弱电解质存在电离平衡,浓度大于盐酸,加水稀释到相同pH,醋酸加入的水多,故B错误;
C、加入硝酸银,会和溴化氢反应生成溴化银浅黄色沉淀溴化银,促进平衡正向进行,溶液颜色变浅,故C正确;
D、弱电解质存在电离平衡,加水稀释促进电离,平衡向电离方向移动,故D正确;
故选:AB.
B、醋酸是弱电解质存在电离平衡,浓度大于盐酸,加水稀释到相同pH,醋酸加入的水多,故B错误;
C、加入硝酸银,会和溴化氢反应生成溴化银浅黄色沉淀溴化银,促进平衡正向进行,溶液颜色变浅,故C正确;
D、弱电解质存在电离平衡,加水稀释促进电离,平衡向电离方向移动,故D正确;
故选:AB.
点评:本题考查了反应自发进行的分析判断,弱电解质的电离平衡,化学平衡的影响因素分析判断,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
下列说法错误的是( )
| A、C2H4和C4H8一定都能使溴水退色 | B、C2H6和C4H10一定是同系物 | C、C3H6不只表示一种物质 | D、烯烃中各同系物中碳的质量分数相同 |
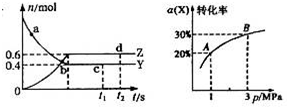 (2013?枣庄二模)一定温度下的密闭容器中发生反应:X(g)+3Y(g)f?2Z(g)△H<0,如图是反应达平衡及改变条件平衡移动的图象.下列说法错误的是( )
(2013?枣庄二模)一定温度下的密闭容器中发生反应:X(g)+3Y(g)f?2Z(g)△H<0,如图是反应达平衡及改变条件平衡移动的图象.下列说法错误的是( )