题目内容
【题目】下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
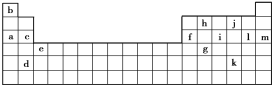
(1)下列________(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)以上13种元素中,____(填写字母)元素原子失去核外第一个电子需要的能量最多。i在周期表中的位置_________。
(3)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:原子核对核外电子的吸引力;形成稳定结构的倾向。
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1);
锂 | X | Y | |
失去第一个电子 | 519 | 502 | 580 |
失去第二个电子 | 7296 | 4570 | 1820 |
失去第三个电子 | 11799 | 6920 | 2750 |
失去第四个电子 | 9550 | 11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量______________。
②表中X可能为以上13种元素中的_____(填写字母)元素。用元素符号表示X和j形成化合物的化学式_____。
③Y是周期表中_____族元素。
【答案】①④ m 第三周期ⅤA族 Li原子失去1个电子后形成稳定结构,此时再失去1个电子很困难 a Na2O和Na2O2 ⅢA
【解析】
(1)金属是导体(锗是半导体),石墨是导体;
(2)越容易失去第一个电子,第一电离能越小;
(3)根据电离能的大小结合原子核外电子排布判断可能的元素种类,注意电离能的大小能判断出元素的化合价,即最外层电子数。
根据元素周期表中元素的分布知识,可以知道a是Na,b是H,c是Mg,d是Sr,e是Sc,f是Al,g是Ge,h是C,j是O,i是P,k是Sb,l是Cl,m是Ar;
(1)金属是电的良导体,石墨棒是电的良导体,金属有Na、Mg、Sr、Sc、Al,锗是半导体,故答案为:①④;
(2)从题目所给信息知道,原子失电子所需能量不仅与原子核对核外电子的吸引力有关,还与形成稳定结构的倾向有关.结构越稳定失电子所需能量越高,在所给13种元素中,处于零族的m元素已达8e-的稳定结构,因此失去核外第一个电子需要的能量最多;i是P,位于元素周期表的第三周期ⅤA族;
(3)①锂原子核外共有3个电子,其中两个在K层,1个在L层,当失去最外层的一个电子后,锂离子处于稳定结构,根据题给信息可知,要使锂离子再失去电子便会形成不稳定结构,因此锂原子失去第二个电子时所需能量远大于失去第一个电子所需的能量;
②由表中数据可知:X失去第2个电子所需能量远大于失去第一个电子所需的能量(9倍多),而失去第三个、第四个电子所需能量皆不足前者的两倍,故第一个电子为最外层的1个电子,而其他几个电子应处于内层;结合所给的周期表知,X应为a,即钠元素,和j即氧元素所形成的化合物化学式分别为Na2O和Na2O2;
③由表中所给Y的数据可知,Y失去第1、2、3个电子所需能量差别不大,而失去第4个电子所需能量远大于失去第3个电子所需的能量,因此Y元素的最外层有3个电子,即为ⅢA族的元素Al。