题目内容
【题目】为了证明在实验室制备得到的Cl2中会混有HCl,甲同学设计了如图所示的实验装置,按要求回答下列问题。
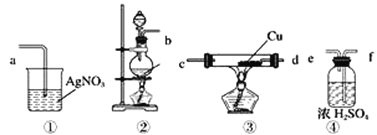
(1)请根据甲同学的示意图,所需实验装置从左至右的连接顺序:装置②→__。
(2)实验室制备Cl2的离子方程式为__。
(3)装置③中Cu的作用__ (用化学方程式表示)。
(4)乙同学认为甲同学实验设计仍然存在缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为此,乙同学提出气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置⑤应放入__。
(5)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成紫色石蕊试液,如果观察到_____的现象,则证明制Cl2时有HCl挥发出来。
【答案】 ④→③→① MnO2+4H++2Cl﹣![]() Mn2++Cl2↑+2H2O Cl2+Cu
Mn2++Cl2↑+2H2O Cl2+Cu![]() CuCl2 湿润的KI-淀粉试纸(或湿润的有色布条) 溶液只变红,不褪色
CuCl2 湿润的KI-淀粉试纸(或湿润的有色布条) 溶液只变红,不褪色
【解析】(1)根据实验目的可以知道,验证实验室制得的Cl2中会混有HCl,因为制得的氯气中除了有氯化氢外还有水蒸汽,所以要先用浓硫酸干燥,再用灼热的铜吸收氯气,然后用硝酸银溶液检验HCl的存在,所以链接顺序为:②![]() ④
④![]() ③
③![]() ①,因此,本题正确答案是:④
①,因此,本题正确答案是:④![]() ③
③![]() ①;
①;
(2)实验室用浓盐酸与二氧化锰加热制氯气,另外还生成氯化锰和水,反应的离子方程式为MnO2+4H++2Cl﹣![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(3)装置③中Cu主要是除去氯气,以便于检验氯化氢,反应方程式为Cl2+Cu![]() CuCl2
CuCl2
(4)根据(1)中的分析可以知道,如果铜没有将氯气完全吸收,最终通入![]() 溶液中产生沉淀的就不一定是氯化氢了,所以为了确保实验结论的可靠性,应排除氯气的干扰,故应检验氯气是否除尽,检验氯气通常用湿润的KI淀粉试纸(或湿润的有色布条),所以气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入AgNO3溶液中的气体只有一种,装置⑤应放入 湿润的KI淀粉试纸(或湿润的有色布条),因此,本题正确答案是:湿润的KI淀粉试纸(或湿润的有色布条);
溶液中产生沉淀的就不一定是氯化氢了,所以为了确保实验结论的可靠性,应排除氯气的干扰,故应检验氯气是否除尽,检验氯气通常用湿润的KI淀粉试纸(或湿润的有色布条),所以气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入AgNO3溶液中的气体只有一种,装置⑤应放入 湿润的KI淀粉试纸(或湿润的有色布条),因此,本题正确答案是:湿润的KI淀粉试纸(或湿润的有色布条);
(5)将原来烧杯中的AgNO溶液换成紫色石蕊试液,如果溶液先变红再褪色,则说明气体中有氯气,如果溶液只变红,不褪色,则说明制Cl2时有HCl挥发出来,因此,本题正确答案是:溶液只变红,不褪色。