题目内容
(8分)1.5 molH3PO4的质量是 ,含有 个H3PO 4分子;同温、同压下等质量的SO2和SO3气体所占的体积比为 ,所含氧元素的质量比为 。
(8分) 147g ; 9.03×1023; 5:4; 5:6 (每空2分)
解析:略

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
下列溶液Cl-的物质的量浓度与50mL 1mol?L-1氯化铝溶液中Cl-的物质的量浓度相等的是( )
| A、150mL 1mol?L-1氯化钠溶液 | B、75mL 1.5 mol?L-1氯化钙溶液 | C、150mL 1mol?L-1氯化钾溶液 | D、50mL 3mol?L-1氯化镁溶液 |
工业上可以从电解铜的阳极泥中提取很多重要物质,其工艺流程如下:
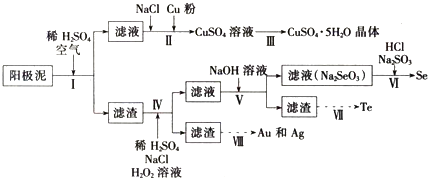
已知:①阳极泥的主要化学成分,如表所示
②温度和硫酸浓度对阳极泥中各组分浸出率的影响,如表所示
(1)步骤I的主要目的为浸出铜,此过程中发生的主要反应的化学方程式为 ,分析表2数据,可知步骤I最适合的条件为 .
(2)步骤Ⅱ中,加入Cu粉的目的是除去滤液中含碲的离子,加入NaCl的目的为 .
(3)步骤Ⅲ的操作方法为 .
(4)步骤Ⅳ中,反应温度为75℃.加入H2O2溶液的作用为 ;此过程中H2O2溶液的添加量要远远高于理沧值,原因为 .
(5)步骤Ⅵ中所发生反应的化学方程式为 .
(6)步骤Ⅶ中,Te的获得可以通过碱性环境下电解Na2TeO3溶液实现,其阴极的电极反应式为 .
(7)步骤Ⅷ中得到的Au和Ag混合物可以用 进行分离(填选项字母).
A.稀硝酸 B.浓盐酸 C.浓氢氡化钠溶液 D.王水.

已知:①阳极泥的主要化学成分,如表所示
| 主要成分 | Cu | Ag | Au | Se | Te |
| 百分含量/% | 23.4 | 12.1 | 0.9 | 6.7 | 3.1 |
| 固定浸出温度 | 固定H2SO4浓度 | |||||||||||
| H2SO4浓度/mol?L-1 | 浸出率/% | 浸出温度/℃ | 浸出率/% | |||||||||
| Cu | Ag | Au | Se | Te | Cu | Ag | Au | Se | Te | |||
| 4 | 95.1 | 4.67 | <0.2 | 0.83 | 8.93 | 30 | 87.1 | 4.58 | <0.2 | 0.08 | 6.83 | |
| 3 | 94.5 | 4.65 | <0.2 | 0.28 | 6.90 | 40 | 94.5 | 4.65 | <0.2 | 0.28 | 6.90 | |
| 2 | 78.1 | 2.65 | <0.2 | 0.05 | 2.85 | 50 | 96.1 | 5.90 | <0.2 | 0.64 | 8.73 | |
(2)步骤Ⅱ中,加入Cu粉的目的是除去滤液中含碲的离子,加入NaCl的目的为
(3)步骤Ⅲ的操作方法为
(4)步骤Ⅳ中,反应温度为75℃.加入H2O2溶液的作用为
(5)步骤Ⅵ中所发生反应的化学方程式为
(6)步骤Ⅶ中,Te的获得可以通过碱性环境下电解Na2TeO3溶液实现,其阴极的电极反应式为
(7)步骤Ⅷ中得到的Au和Ag混合物可以用
A.稀硝酸 B.浓盐酸 C.浓氢氡化钠溶液 D.王水.



