题目内容
(Ⅰ)从海水中可提取各种化工原料.如图是工业上对海水综合利用的示意图如图1.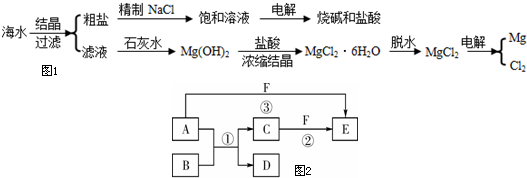
试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时需用四种试剂,使上述离子逐一沉淀,加入试剂的顺序是:NaOH溶液→①
(2)由MgCl2?6H2O晶体脱水制无水MgCl2时,需要控制的条件是
(Ⅱ)A、B、C、D、E、F六种物质的相互转化关系如图2所示(反应条件未标出),其中反应①是置换反应.
(1)若A、D、F都是短周期元素组成的非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是
(2)若A、D、F都是单质,且A为金属,F为黄绿色气体,则反应②的离子方程式是
分析:(Ⅰ)(1)根据根据SO42-、Ca 2+、Mg2+等易转化为沉淀而被除去,以及根据不能产生新杂质的要求排序,前面加入的过量溶液应用后加入的溶液除去,最后加入盐酸溶液.
(2)从MgCl2?6H2O制无水MgCl2时加热会促进镁离子的水解生成氢氧化镁和氯化氢,加入HCl气体,抑制水解;
(Ⅱ)(1)由反应①A+B→C+D,C+Cl2→E,结合A是常见的非金属单质,D是非金属单质,反应①是置换反应,考虑反应①是C与二氧化硅发生的置换反应,A、F所含元素同周期,则F为氧气,所以A为碳,B为二氧化硅,C为一氧化碳,D为硅,F为氧气,E为二氧化碳;
(2)F是黄绿色气态单质,为Cl2,由反应①A+B→C+D,C+Cl2→E,结合A是常见的金属单质,D是金属单质,反应①是置换反应,考虑反应①是金属与盐发生的置换反应,C含有金属A的元素,由C
E,A
E可知,A为变价金属,故A为Fe,C为FeCl2,E为FeCl3;
(2)从MgCl2?6H2O制无水MgCl2时加热会促进镁离子的水解生成氢氧化镁和氯化氢,加入HCl气体,抑制水解;
(Ⅱ)(1)由反应①A+B→C+D,C+Cl2→E,结合A是常见的非金属单质,D是非金属单质,反应①是置换反应,考虑反应①是C与二氧化硅发生的置换反应,A、F所含元素同周期,则F为氧气,所以A为碳,B为二氧化硅,C为一氧化碳,D为硅,F为氧气,E为二氧化碳;
(2)F是黄绿色气态单质,为Cl2,由反应①A+B→C+D,C+Cl2→E,结合A是常见的金属单质,D是金属单质,反应①是置换反应,考虑反应①是金属与盐发生的置换反应,C含有金属A的元素,由C
| 氯气 |
| 氯气 |
解答:解:(Ⅰ)(1)SO42-、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应先加BaCl2溶液再加Na2CO3溶液,最后加入盐酸;
故答案为:BaCl2溶液;Na2CO3溶液;
(2)从MgCl2?6H2O制无水MgCl2操作时 需要加热,加热会促进镁离子的水解生成氢氧化镁和氯化氢,方程式为:MgCl2?6H2O
Mg(OH)2+2HCl+4H2O,为了防止水解,加入HCl气体,使水解平衡逆向移动,抑制水解;
故答案为:HCl;MgCl2?6H2O
Mg(OH)2+2HCl+4H2O;
(Ⅱ)(1)由反应①A+B→C+D,C+Cl2→E,结合A是常见的非金属单质,D是非金属单质,反应①是置换反应,考虑反应①是C与二氧化硅发生的置换反应,方程式为:2C+SiO2
Si+2CO;
故答案为:2C+SiO2
Si+2CO;
(2)F是黄绿色气态单质,为Cl2,由反应①A+B→C+D,C+Cl2→E,结合A是常见的金属单质,D是金属单质,反应①是置换反应,考虑反应①是金属与盐发生的置换反应,C含有金属A的元素,由C
E,A
E可知,A为变价金属,故A为Fe,反应②为:2FeCl2+Cl2═2FeCl3,离子方程式为:2Fe2++Cl2═2Fe3++2Cl-;
故答案为:2Fe2++Cl2═2Fe3++2Cl-;
故答案为:BaCl2溶液;Na2CO3溶液;
(2)从MgCl2?6H2O制无水MgCl2操作时 需要加热,加热会促进镁离子的水解生成氢氧化镁和氯化氢,方程式为:MgCl2?6H2O
| ||
故答案为:HCl;MgCl2?6H2O
| ||
(Ⅱ)(1)由反应①A+B→C+D,C+Cl2→E,结合A是常见的非金属单质,D是非金属单质,反应①是置换反应,考虑反应①是C与二氧化硅发生的置换反应,方程式为:2C+SiO2
| ||
故答案为:2C+SiO2
| ||
(2)F是黄绿色气态单质,为Cl2,由反应①A+B→C+D,C+Cl2→E,结合A是常见的金属单质,D是金属单质,反应①是置换反应,考虑反应①是金属与盐发生的置换反应,C含有金属A的元素,由C
| 氯气 |
| 氯气 |
故答案为:2Fe2++Cl2═2Fe3++2Cl-;
点评:本题主要考查了粗盐的提纯以及框图推断题,框图推断题关键抓住题目的突破口,难度较大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
化学与生产、生活、社会密切相关.下列有关说法中不正确的是( )
| A、2008年北京奥运会开幕式上的“脚印”等焰火让全世界为之欢呼、倾倒,这主要是利用了化学中“焰色反应”的有关知识 | B、神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 | C、腌制食品中应严格控制NaNO2的用量 | D、从海水中可提取Mg,用惰性电极电解熔融的MgCl2或其水溶液都可制得Mg |