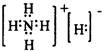题目内容
已知将盐酸滴入酸性高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去.现有一个氧化还原反应的体系中共有HCl、Cl2、H2O、KMnO4、MnCl2、KCl六种物质:
(1)写出一个包含上述六种物质的配平的氧化还原反应方程式,并用单线桥标出电子转移方向和数目:________.
(2)上述反应中,氧化剂是________,1 mol氧化剂在反应中得到的电子数目为________;生成的氧化产物的物质的量为________.
(3)如果在反应后的溶液中加入NaBiO3,溶液又变紫红色.说出NaBiO3的一个性质:________.
答案:
解析:
解析:
|
(1) (2)KMnO4 5NA 2.5 mol (3)NaBiO3具有强氧化性(比KMnO4氧化性强) |

练习册系列答案
相关题目