题目内容
含有下列各组离子的溶液中,通入足量SO2气体后仍能大量共存的是( )
| A、H+、Ca2+、Al3+、NO3- |
| B、Ba2+、K+、Na+、OH- |
| C、Na+、NH4+、I-、S2- |
| D、Na+、Ca2+、K+、Cl- |
考点:离子共存问题
专题:离子反应专题
分析:A.硝酸根离子在氢离子电离大量存在条件下具有强氧化性,能够氧化二氧化硫;
B.二氧化硫与氢氧根离子反应生成亚硫酸根离子,亚硫酸根离子与钡离子反应生成亚硫酸钡沉淀;
C.二氧化硫在溶液中与硫离子反应生成硫单质;
D.四种离子之间不发生反应,通入二氧化硫后也不反应
B.二氧化硫与氢氧根离子反应生成亚硫酸根离子,亚硫酸根离子与钡离子反应生成亚硫酸钡沉淀;
C.二氧化硫在溶液中与硫离子反应生成硫单质;
D.四种离子之间不发生反应,通入二氧化硫后也不反应
解答:
解:A.H+、NO3-能够氧化二氧化硫,在溶液中不能大量共存,故A错误;
B.Ba2+、OH-与二氧化硫反应生成亚硫酸钡,在溶液中不能大量共存,故B错误;
C.S2-、SO2反应生成S单质,在溶液中不能大量共存,故C错误;
D.Na+、Ca2+、K+、Cl-离子之间不发生反应,通入二氧化硫也不反应,在溶液中能够大量共存,故D正确;
故选D.
B.Ba2+、OH-与二氧化硫反应生成亚硫酸钡,在溶液中不能大量共存,故B错误;
C.S2-、SO2反应生成S单质,在溶液中不能大量共存,故C错误;
D.Na+、Ca2+、K+、Cl-离子之间不发生反应,通入二氧化硫也不反应,在溶液中能够大量共存,故D正确;
故选D.
点评:本题考查离子共存的判断,为中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;是“可能”共存,还是“一定”共存等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列有关说法错误的是( )
A、 既可以表示10B的原子结构,也可以表示11B的原子结构 既可以表示10B的原子结构,也可以表示11B的原子结构 |
| B、H++OH-=H2O既可以表示NaOH与盐酸反应,也可以表示Ba(OH)2与硫酸反应 |
| C、CH4分子的空间结构与NH4+的相同 |
| D、C2H4O2既可以表示乙酸的分子式,也可以表示甲酸甲酯的分子式 |
下列各组离子在溶液中能大量共存的是( )
| A、Na+、OH-、S2O32-、Cl- |
| B、Fe2+、K+、[Fe(CN)6]3-、NO3- |
| C、H+、C2O42-、MnO4-、SO42- |
| D、Na+、Ca2+、AlO2-、HCO3- |
化学与环境、生产和生活等密切相关,下列说法正确的是( )
| A、明矾是一种水处理剂,可用于水的杀菌、消毒 |
| B、用食醋可除去水壶内壁上的水垢 |
| C、因花中有芳香醇因此才闻到花香 |
| D、pH小于7的雨水即为酸雨 |
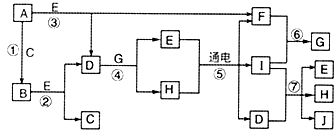 A-J是中学化学常见的几种物质,它们之间的转化关系如图所示.已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F合成,J可用作杀菌消毒剂.回答下列问题:
A-J是中学化学常见的几种物质,它们之间的转化关系如图所示.已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F合成,J可用作杀菌消毒剂.回答下列问题: