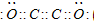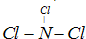��Ŀ����
����A��B��C��D��E����ǿ����ʣ�������ˮ�пɵ�������������ӣ��������Ӳ��ظ�����
| ������ | H+��Na+��A13+��Ag+��Ba2+ |
| ������ | OH����C1����CO32-��NO3����SO42- |
��֪��
��A��B����Һ�ʼ��ԣ�C��D��E��Һ�����ԡ�
��A��Һ��E��Һ��Ӧ�����������г���������A��Һ��C��Һ��Ӧֻ������������������������ͬ����
��D��Һ������������Һ��Ӧ���ܲ���������Cֻ����D��Ӧ����������
�Իش��������⣺
��1����C��Һ��μ��������������ʵ�����Ũ�ȵ�A��Һ�У���Ӧ����Һ�и�������Ũ���ɴ�С��˳��Ϊ�� ��
��2��д��E��Һ�������B��Һ��Ӧ�����ӷ���ʽ ��
��3����֪��NaOH��aq��+HNO3��aq��= NaNO3��aq��+H2O(1);��H=��a KJ��mol-1����д��B��C��ϡ��Һ��Ӧ���Ȼ�ѧ����ʽ ��
��4����100mL0.1mol��L-1E��Һ�У���μ���35mL 2mol��L-1NaOH��Һ�����յõ��������ʵ���Ϊ ��
��1��c��Na+��>c��C1����>c��HCO3����>c��OH����>c��H+��> c��CO32����
��c��Na+��>c��C1����>c��HCO3����>c��OH����>c��H+��
��2��2A13+ + 3SO2-4 +3Ba2+ + 8OH = 2A1O2�� + 3BaSO4��+ 4H2O
��3��OH����aq��+H+��aq��= H2O��1������H =-aKJ/mol
(���ʾۼ�״̬����Ӧ����һ������������֣���4��0.01mol

 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д�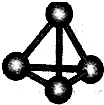 ����A��B��C��D��E��F���ֶ�����Ԫ�أ����ǵ�ԭ��������������D��E���⻯����ӹ��Ͷ���V�ͣ�A��B������������֮����C��������������ȣ�A�ֱܷ���B��C��D�γɵ���������ȵķ��ӣ���A��D���γɵĻ���������¾�ΪҺ̬��
����A��B��C��D��E��F���ֶ�����Ԫ�أ����ǵ�ԭ��������������D��E���⻯����ӹ��Ͷ���V�ͣ�A��B������������֮����C��������������ȣ�A�ֱܷ���B��C��D�γɵ���������ȵķ��ӣ���A��D���γɵĻ���������¾�ΪҺ̬��