题目内容
5.(1)写出下列物质的电子式:①NH4Cl ②Na2O2 ③CO2 ;
; ;
;
(2)用电子式表示下列物质的形成过程:①MgCl2
 ②H2O22H•+2
②H2O22H•+2 →
→ .
.
分析 (1)①NH4Cl氯是离子化合物,由氨根离子与氯离子构成,铵根离子内氮原子与氢原子通过共价键结合;
②Na2O2 是离子化合物,2个钠离子与1个过氧根离子构成,过氧根离子内部存在O-O共价键;
③CO2是共价化合物,二氧化碳中存在两对碳氧共用电子对;
(2)氯化镁为离子化合物,是由镁离子与2个氯离子通过离子键结合而成;
过氧化氢为共价化合物,两个氧原子通过共用电子对形成O-O,两个氧原子分别与两个氢原子通过共用电子对形成H-O键.
解答 解:(1)①氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为: ;
;
②Na2O2是离子化合物,由Na+离子和O2-离子构成,Na2O2的电子式为: ;
;
③CO2是共价化合物,二氧化碳中存在两对碳氧共用电子对,电子式为: ;
;
故答案为: ;
; ;
; ;
;
(2)①氯化镁为离子化合物,是由镁离子与2个氯离子通过离子键结合而成,其形成过程为: ;
;
故答案为: ;
;
②过氧化氢为共价化合物,两个氧原子通过共用电子对形成O-O,两个氧原子分别与两个氢原子通过共用电子对形成H-O键,其形成过程为:2H•+2 →
→ ;
;
故答案为:2H•+2 →
→ .
.
点评 本题考查了电子式的书写,掌握电子式的概念及表示方法,明确离子化合物与共价化合物的电子式的表示方法,题目难度不大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
15.有关SO2说法错误的是( )
| A. | 单质硫在空气中燃烧可生成SO2 | |
| B. | SO2能使品红溶液褪色,加热可恢复红色 | |
| C. | SO2能使加酚酞的NaOH溶液褪色是因为它能与NaOH反应 | |
| D. | SO2和Cl2都具有漂白作用,所以将两种气体同时作用于潮湿有色物,可大大增强漂白作用 |
16.下列物质中,在一定条件下不能与乙烯发生加成反应的是( )
| A. | 氢气 | B. | 水 | ||
| C. | 氧气 | D. | 溴的四氯化碳溶液 |
10.将1.01g固体KNO3溶解在热的稀硫酸中,当加入30mL 0.5mol•L-1K2S溶液时,两者恰好反应完,放出NxOy气体,下列叙述正确的是( )
| A. | 氧化剂与还原剂物质的量之比为3:2 | |
| B. | 当S2-全部转化成S时,x=1,y=2 | |
| C. | 反应转移0.03mol电子 | |
| D. | 当S2-全部转化成S和SO2时,氧化产物为0.015mol |
14.下列各式用电子式表示的物质的形成过程,其中正确的是( )
| A. | 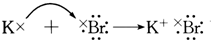 | |
| B. | 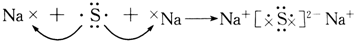 | |
| C. | 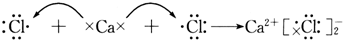 | |
| D. | 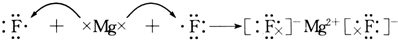 |