题目内容
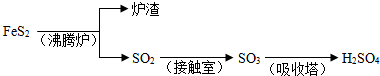
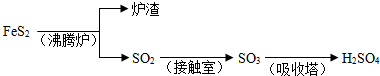
工业上由FeS2制H2SO4的转化关系如下:?
![]()
①SO2在接触室中反应的平衡转化率与压强、温度的关系如下表(MPa=106Pa):?
 根据化学平衡理论和上表数据,考虑综合经济效益,接触室中的反应压强宜
根据化学平衡理论和上表数据,考虑综合经济效益,接触室中的反应压强宜
选择 MPa;而反应温度选定400~500 ℃的理由是 。?
②往体积相同的甲、乙两个容器中,分别充入等物质的量的SO2和O2,在相同温度下发生反应,反应过程中,甲容器保持体积不变,乙容器保持压强不变,当反应达到平衡时,甲容器中SO2的转化率 (填“>”“=”或“<”)乙容器中SO2的转化率。?
(2)考虑综合经济效益,当炉渣中含铁量大于45%时,可用于炼铁、制造硫酸亚铁等。?
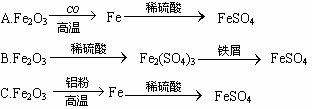
①利用炉渣里的Fe2O3制FeSO4的方案中,最可行的是 (填标号)。?
②FeSO4·7H2O是水处理的常用凝聚剂。净水过程中Fe2+经氧化水解生成 ,净水的原理是 ?
(1)①0.1?
催化剂活性最高且反应速率和SO2平衡转化率较理想?
②<?
(2)①B?
②Fe(OH)3胶体?
生成的胶体吸附水中悬浮物质并使之沉降?
解析:(1)①由于不同压强条件下SO2转化率都较高,故选择标准大气压0.1 MPa。?
400~500 ℃时催化剂活性大且速率和SO2平衡转化率均较高。?
②设都保持等压,达平衡时SO2转化率相同,而2SO2 + O2![]() 2SO3为物质的量减少的反应,故随反应进行,气体体积应减少,若要恢复至等容需扩大容积减小压强,平衡则左移。?
2SO3为物质的量减少的反应,故随反应进行,气体体积应减少,若要恢复至等容需扩大容积减小压强,平衡则左移。?
(2)①A与B相比消耗了大量能量。C也消耗大量能量且生成Fe易不纯。?
②Fe3+ + 3H2O![]() Fe(OH)3 + 3H+,产生Fe(OH)3为胶体,有较大表面积,有吸附作用。
Fe(OH)3 + 3H+,产生Fe(OH)3为胶体,有较大表面积,有吸附作用。

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
工业上由FeS2制H2SO4的转化关系如下:

填写下列空白:
(1)吸收塔中发生反应的化学方程式为______.
(2)接触室内发生的反应为:SO2(g)+ O2(g)
O2(g) SO3(g)△H=a kJ?mol-1 下表为不同温度(T)下该反应的化学平衡常数(K):
SO3(g)△H=a kJ?mol-1 下表为不同温度(T)下该反应的化学平衡常数(K):
| T/K | 673 | 723 | 823 | 923 |
| K | 423 | 37.4 | 20.5 | 4.68 |
②K值越大,表明反应达到平衡时______(填标号).
A.SO2的转化率一定越高 B.SO3的产量一定越大
C.正反应进行得越完全 D.化学反应速率越大
(3)考虑综合经济效益,当炉渣含铁量大于45%时,可用于制硫酸亚铁等.下列利用炉渣里的Fe2O3制FeSO4的方案中,最能体现绿色化学理念的方案是______(填标号)
A.Fe2O3
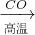 Fe
Fe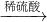 FeSO4
FeSO4B.Fe2O3
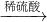 Fe2(SO4)3
Fe2(SO4)3 FeSO
FeSO C.Fe2O3
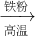 Fe
Fe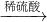 FeSO4
FeSO4D.Fe2O3
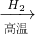 Fe
Fe FeSO4
FeSO4(4)为实现绿色环保、节能减排和废物利用等目的,某硫酸厂用碳酸钙作吸收剂与水配成浆液,洗涤尾气(SO2的体积分数为0.200%)并吸收SO2,得到石膏(CaSO4?2H2O).求:22.4m3(标准状况下)的尾气可制得石膏多少千克?(设二氧化硫的利用率为80.0%)
工业上由FeS2制H2SO4的转化关系如下:

填写下列空白:
(1)已知吸收塔中每40gSO3气体被水完全吸收生成液态硫酸放出65.15kJ,写出该反应的热化学方程式______;
(2)接触室内发生的反应为:
SO2(g)+ O2(g)
O2(g)  SO3(g)△H=a kJ?mol-1
SO3(g)△H=a kJ?mol-1
下表为不同温度(T)下该反应的化学平衡常数(K):
①根据上表数据及化学平衡理论,上述反应中a______0(填“>”或“<”);
②K值越大,表明反应达到平衡时______(填标号).
A.SO2的转化率一定越高 B.SO3的产量一定越大
C.正反应进行得越完全 D.化学反应速率越大
(3)考虑综合经济效益,当炉渣含铁量大于45%时,可用于制硫酸亚铁等.下列利用炉渣里的Fe2O3制FeSO4的方案中,最能体现绿色化学理念的方案是______(填标号);
A.Fe2O3 Fe
Fe FeSO4;B.Fe2O3
FeSO4;B.Fe2O3 Fe2(SO4)3
Fe2(SO4)3 FeSO4;C.Fe2O3
FeSO4;C.Fe2O3 Fe
Fe FeSO4
FeSO4
(4)为了探究接触室里催化剂颗粒(粗颗粒和细颗粒),反应的温度(673K和723K),反应的压强(101Kpa和1010Kpa)对反应速率的影响,通过变换这些实验条件,至少需要完成______个实验然后进行对比得出结论;
(5)为实现绿色环保、节能减排和废物利用等目的,某硫酸厂用碳酸钙作吸收剂与水配成浆液,洗涤尾气(SO2的体积分数为0.200%)并吸收SO2,得到石膏.求:22.4m3(标准状况下)的尾气可制得石膏______千克;(取两位有效数字)(设二氧化硫的利用率为80.0% )
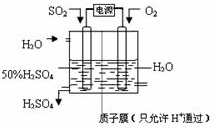
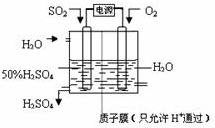
(6)科学家研究出以图所示装置用电化学原理生产硫酸的新工艺,其阳极的电极反应式为______,总反应的化学方程式为______.


填写下列空白:
(1)已知吸收塔中每40gSO3气体被水完全吸收生成液态硫酸放出65.15kJ,写出该反应的热化学方程式______;
(2)接触室内发生的反应为:
SO2(g)+
 O2(g)
O2(g)  SO3(g)△H=a kJ?mol-1
SO3(g)△H=a kJ?mol-1下表为不同温度(T)下该反应的化学平衡常数(K):
| T/K | 673 | 723 | 823 | 923 |
| K | 423 | 37.4 | 20.5 | 4.68 |
②K值越大,表明反应达到平衡时______(填标号).
A.SO2的转化率一定越高 B.SO3的产量一定越大
C.正反应进行得越完全 D.化学反应速率越大
(3)考虑综合经济效益,当炉渣含铁量大于45%时,可用于制硫酸亚铁等.下列利用炉渣里的Fe2O3制FeSO4的方案中,最能体现绿色化学理念的方案是______(填标号);
A.Fe2O3
 Fe
Fe FeSO4;B.Fe2O3
FeSO4;B.Fe2O3 Fe2(SO4)3
Fe2(SO4)3 FeSO4;C.Fe2O3
FeSO4;C.Fe2O3 Fe
Fe FeSO4
FeSO4(4)为了探究接触室里催化剂颗粒(粗颗粒和细颗粒),反应的温度(673K和723K),反应的压强(101Kpa和1010Kpa)对反应速率的影响,通过变换这些实验条件,至少需要完成______个实验然后进行对比得出结论;
(5)为实现绿色环保、节能减排和废物利用等目的,某硫酸厂用碳酸钙作吸收剂与水配成浆液,洗涤尾气(SO2的体积分数为0.200%)并吸收SO2,得到石膏.求:22.4m3(标准状况下)的尾气可制得石膏______千克;(取两位有效数字)(设二氧化硫的利用率为80.0% )
(6)科学家研究出以图所示装置用电化学原理生产硫酸的新工艺,其阳极的电极反应式为______,总反应的化学方程式为______.