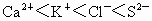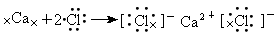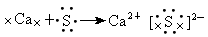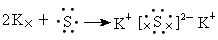题目内容
有A、B、C、D四种元素,A的正二价离子与氩原子的电子层结构相同,B原子有三个电子层,其单质为双原子分子,C的核外电子比A少一个,B与D同周期,其单质为淡黄色固体.
(1)写出A、B、C、D的离子符号
(2)A、B、C、D的离子半径由小到大的顺序是怎样的?
(3)用电子式表示这四种元素中两两形成离子化合物的过程.
答案:略
解析:
提示:
解析:
|
(1)A 、B、C、D的离子符号应分别为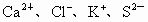
(2) (3)
|
提示:
|
有三个电子层,为第三周期,第三周期元素的单质能形成双原子分子的只有氯元素,所以 B为Cl;C的核外电子比A少一个,应是K;D与B同周期,单质为淡黄色,应为S.此题易出现的错误是: (1) 将离子符号写成元素符号;(2) 将离子半径大小顺序写反;(3) 书写电子式不规范. |

练习册系列答案
相关题目