题目内容
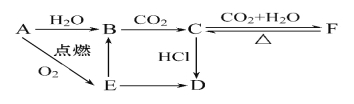
【题目】A、B、C、D、E、F六种物质有如下变化关系,E是淡黄色粉末,判断:
(1)写出B、C、D、F的化学式:
B. C. D. F. 。
(2)写出有关反应的离子方程式
B→C: ________________________________,
E→B: _______________________________,
F→C: _______________________________。
【答案】(1)NaOHNa2CO3NaClNaHCO3
(2)2OH-+CO2=CO32-+H2O
2Na2O2+2H2O=4Na++4OH-+O2↑
2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
【解析】
试题分析:E是淡黄色粉末,A燃烧生成E,所以A是Na,E是过氧化钠,钠和水反应生成氢氧化钠,则B是氢氧化钠,氢氧化钠吸收CO2生成C是碳酸钠,碳酸钠继续吸收CO2转化为碳酸氢钠,即F是碳酸氢钠,碳酸氢钠受热分解生成碳酸钠。碳酸钠与盐酸反应生成D,过氧化钠和盐酸反应也生成D,所以D是氯化钠。
(1)根据以上分析可知B、C、D、F的化学式分别是NaOH、Na2CO3、NaCl、NaHCO3;
(2)根据以上分析可知B→C的方程式为2OH-+CO2=CO32-+H2O;E→B的方程式为2Na2O2+2H2O=4Na++4OH-+O2↑;F→C的方程式为2NaHCO3![]() Na2CO3+H2O+CO2↑。
Na2CO3+H2O+CO2↑。

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目