题目内容
归纳法是髙中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:(均在常温下)
①pH=1的强酸溶液,加水稀释后,溶液中离子浓度都降低。
②pH=2的盐酸和pH=l的盐酸,c(H+)之比为2 :1
③pH相等的三种溶液:a.CH3COONa b.NaHCO3 c.NaOH,其溶质物质的量浓度由小到大顺序为:c、b、a
④反应2A(s)+B (g)="2C" (g)+D (g)不能自发进行,则该反应△H一定大于0
⑤已知醋酸电离平衡常数为Ka,醋酸根水解常数为Kb,水的离子积为Kw,则三者关系为:Ka·Kb=Kw
⑥反应A(g)="2" B (g) △H,若正反应的活化能为Ea kJ·mol-1,逆反应的活化能为Eb kJ.mol-1,则△H=(Ea-Eb)kJ·mol-1
上述归纳正确的是
- A.全部
- B.③④⑤⑥
- C.②④⑤⑥
- D.①②④⑤
B
试题分析:加水稀释后,酸中的c(H+)减小,但溶液中的c(OH-)增大,①错;pH=2的酸c(H+)=10-2mol·L-1,pH=1的酸c(H+)=10-1mol·L-1,c(H+)之比为1:10,②错;CH3COONa、NaHCO3溶液水解后显碱性,但HCO3-的水解程度大于CH3COO-,因此pH相等时NaHCO3溶液浓度小,NaOH是强碱,相同pH时浓度最小,③正确;该反应是熵增的反应,不能自发进行则△H一定大于0,④正确;醋酸的电离平衡常数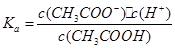 ,醋酸跟的水解常数
,醋酸跟的水解常数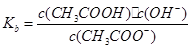 ,则Ka·Kb= c(H+)·c(OH-)=Kw,⑤正确;正反应的活化能为反应物断裂化学键吸收的能量,逆反应的活化能为生成物形成化学键释放的能量,故反应热正反应活化能减去逆反应活化能,⑥正确。
,则Ka·Kb= c(H+)·c(OH-)=Kw,⑤正确;正反应的活化能为反应物断裂化学键吸收的能量,逆反应的活化能为生成物形成化学键释放的能量,故反应热正反应活化能减去逆反应活化能,⑥正确。
考点:考查溶液稀释,pH计算,盐类水解,反应进行的方向,平衡常数,反应热计算等内容。
试题分析:加水稀释后,酸中的c(H+)减小,但溶液中的c(OH-)增大,①错;pH=2的酸c(H+)=10-2mol·L-1,pH=1的酸c(H+)=10-1mol·L-1,c(H+)之比为1:10,②错;CH3COONa、NaHCO3溶液水解后显碱性,但HCO3-的水解程度大于CH3COO-,因此pH相等时NaHCO3溶液浓度小,NaOH是强碱,相同pH时浓度最小,③正确;该反应是熵增的反应,不能自发进行则△H一定大于0,④正确;醋酸的电离平衡常数
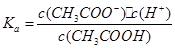 ,醋酸跟的水解常数
,醋酸跟的水解常数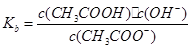 ,则Ka·Kb= c(H+)·c(OH-)=Kw,⑤正确;正反应的活化能为反应物断裂化学键吸收的能量,逆反应的活化能为生成物形成化学键释放的能量,故反应热正反应活化能减去逆反应活化能,⑥正确。
,则Ka·Kb= c(H+)·c(OH-)=Kw,⑤正确;正反应的活化能为反应物断裂化学键吸收的能量,逆反应的活化能为生成物形成化学键释放的能量,故反应热正反应活化能减去逆反应活化能,⑥正确。考点:考查溶液稀释,pH计算,盐类水解,反应进行的方向,平衡常数,反应热计算等内容。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目