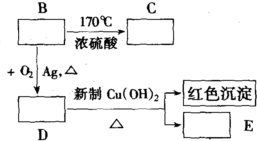
题目内容
4.下列反应中硫酸既表现出了强氧化性又表现了酸性的是( )| A. | 氧化铜与硫酸反应 | B. | 氢氧化铝与硫酸反应 | ||
| C. | 木炭粉与浓硫酸反应 | D. | 铜与浓硫酸反应 |
分析 硫酸既能表现出酸性又表现出氧化性,在反应中应生成硫酸盐,且硫酸被还原生成二氧化硫等物质,据此解答.
解答 解:A.氧化铜与硫酸反应生成硫酸铜和水,只表现硫酸的酸性,故A不选;
B.氢氧化铝与硫酸反应生成硫酸铝和水,只表现硫酸的酸性,故B不选;
C.木炭粉与浓硫酸反应生成二氧化碳和二氧化硫、水,只表示硫酸的强氧化性,故C不选;
D.铜与浓硫酸反应生成硫酸铜、二氧化硫和水,硫酸既表现出了强氧化性又表现了酸性,故D选;
故选:D.
点评 本题考查了元素化合物知识,熟悉硫酸的强氧化性、酸性是解题关键,题目难度不大.

练习册系列答案
相关题目
14.某烷烃的式量为72,跟Cl2反应生成的一卤代物只有一种,该烷烃是( )
| A. | 戊烷 | B. | 乙烷 | C. | 2-甲基丁烷 | D. | 2,2-二甲基丙烷 |
15.下列关于碱金属元素和卤素的说法中,错误的是( )
| A. | 钾与水的反应比钠与水的反应更剧烈 | |
| B. | 溴单质与水的反应比氯单质与水的反应更剧烈 | |
| C. | 随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大 | |
| D. | 碱金属元素中,锂原子失去最外层电子的能力最弱 |
19.欲迅速除去铁壶底的水垢,最好的办法是用( )
| A. | 浓盐酸 | B. | 稀硝酸 | C. | 浓硫酸 | D. | 浓硝酸 |
9.下列有关盐酸、硝酸、硫酸的叙述正确的是( )
| A. | 都是无色液体 | B. | 都是易挥发有刺激性气味的液体 | ||
| C. | 浓溶液在空气中都有白雾生成 | D. | 都是易溶于水的强酸 |
16.设NA为阿伏伽德罗常数的数值,下列叙述不正确的是( )
| A. | 标准状况下,4.4g CO2中含有的原子数为0.3NA | |
| B. | 标准状况下,22.4L甲烷中含有的C-H键数为4NA | |
| C. | 5.6g 铁粉与硝酸反应失去的电子数可能为0.25NA | |
| D. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1 mol•L-1 |
9.下列实验能达到实验预期的是( )
| 选项 | 实验内容 | 实验目的 |
| A | 向1mL0.2mol/LNaOH溶液中滴入2滴0.1mol/LMgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同条件下溶解度Mg(OH)2>Fe(OH)3 |
| B | 过量的铁粉中加入稀硝酸,充分反应后,滴入KSCN溶液,溶液不呈红色 | 证明稀硝酸不能将铁氧化为Fe3+ |
| C | 向淀粉水解液中加入新制Cu(OH)2,煮沸,没有生成砖红色沉淀 | 淀粉没有水解 |
| D | 向混有BaCO3沉淀的NaOH溶液中滴入已知浓度的盐酸(用酚酞作指示剂) | 滴定其中NaOH含量 |
| A. | A | B. | B | C. | C | D. | D |