题目内容
4.下列5种不同粒子 11H、12H、13H、614C、53125I表示3种元素,5种核素,11H、12H、13H互称为同位素.分析 根据元素的种类由质子数决定分析,根据质子数、中子数和核数、同位素的概念判断,具有相同质子数,不同中子数同一元素的不同核素互为同位素.
解答 解:元素就是具有相同的核电荷数(即核内质子数)的一类原子的总称,不同种元素最本质的区别是质子数不同,元素的种类由质子数决定,11H、12H、13H的质子数都是1,所以3种不同粒子${\;}_{1}^{1}H$、${\;}_{1}^{2}H$、${\;}_{1}^{3}H$表示同一种元素氢元素;${\;}_{6}^{14}C$表示碳元素,${\;}_{53}^{125}I$表示碘元素,故总共有3种元素;
核素是指具有一定数目质子和一定数目中子的一种原子;11H、12H、13H的质子数都是1,中子数分别为0、1、2,属于三种核数,;${\;}_{6}^{14}C$表示碳的一种核素,${\;}_{53}^{125}I$表示碘元素的一种核素,故总共有5种核素;
具有相同质子数,不同中子数同一元素的不同核素互为同位素;11H、12H、13H的质子数都是1,中子数分别为0、1、2,属于同位素;
故答案为:3;5;同位素.
点评 本题主要考查的是元素的概念、核素的概念以及同位素的概念,难度不大.

练习册系列答案
相关题目
14.结晶玫瑰是具有强烈玫瑰香气的香料,化学式为C10H9O2Cl3.它属于( )
| A. | 无机物 | B. | 有机物 | C. | 单质 | D. | 混合物 |
12.下表是元素周期表的一部分,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为 ;
;
(2)写出①元素的单质分子的电子式 ;用电子式表示元素②与⑪化合物的形成过程
;用电子式表示元素②与⑪化合物的形成过程 ,该化合物属于共价(填“共价”或“离子”)化合物.
,该化合物属于共价(填“共价”或“离子”)化合物.
(3)碱性最强的化合物的电子式是: ;
;
(4)②元素氢化物在常温下和③发生反应所得溶液的pH>7
(5)元素③与 ⑩形成化合物的化学式是NaCl,高温灼烧该化合物时,火焰呈黄色.
(6)元素⑦与⑩两者核电荷数之差是18.
(7)比较元素⑦、⑨、⑩原子的半径大小K>Br>Cl
(8)③④⑤单质的活泼性顺序为:Na>Mg>Al(从大到小,判断的实验依据是:与酸反应的剧烈程度(任写一种)
(9)请设计一个实验方案,比较⑦和⑩单质氧化性的强弱:Cl2+2Br-=Br2+2Cl-.
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VⅡA | 0 |
| 二 | ⑪ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 ;
;(2)写出①元素的单质分子的电子式
 ;用电子式表示元素②与⑪化合物的形成过程
;用电子式表示元素②与⑪化合物的形成过程 ,该化合物属于共价(填“共价”或“离子”)化合物.
,该化合物属于共价(填“共价”或“离子”)化合物.(3)碱性最强的化合物的电子式是:
 ;
;(4)②元素氢化物在常温下和③发生反应所得溶液的pH>7
(5)元素③与 ⑩形成化合物的化学式是NaCl,高温灼烧该化合物时,火焰呈黄色.
(6)元素⑦与⑩两者核电荷数之差是18.
(7)比较元素⑦、⑨、⑩原子的半径大小K>Br>Cl
(8)③④⑤单质的活泼性顺序为:Na>Mg>Al(从大到小,判断的实验依据是:与酸反应的剧烈程度(任写一种)
(9)请设计一个实验方案,比较⑦和⑩单质氧化性的强弱:Cl2+2Br-=Br2+2Cl-.
19.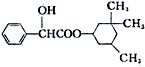 环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物质的叙述中,正确的是( )
环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物质的叙述中,正确的是( )
 环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物质的叙述中,正确的是( )
环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如图.下列对该物质的叙述中,正确的是( )| A. | 该物质属于芳香烃 | |
| B. | 该有机物不能被氧化成醛 | |
| C. | 分子式为C17H23O3 | |
| D. | 1mol该物质最多可与2 mol NaOH发生反应 |
9.下列物质中,不能使酸性KMnO4溶液褪色的是( )
①乙烯 ②甲烷 ③乙苯 ④乙炔 ⑤苯酚 ⑥甲苯 ⑦苯 ⑧乙醇.
①乙烯 ②甲烷 ③乙苯 ④乙炔 ⑤苯酚 ⑥甲苯 ⑦苯 ⑧乙醇.
| A. | ②③④⑥ | B. | ②③④⑤⑥⑦⑧ | C. | ②④⑦ | D. | ②⑦ |
16.对于可逆反应4NH3+5O2?4NO+6H2O(g),下列叙述正确的是( )
| A. | 只有达到平衡时,消耗O2的速率与生成NO的速率之比才为5;4 | |
| B. | 若单位时间生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态 | |
| C. | 达到平衡状态后,NH3、O2、NO、H2O(g)的物质的量保持不变 | |
| D. | 达到平衡状态时,若增加容器体积,则反应速率增大 |
 .
.