��Ŀ����
����������Ҫ�ɷ�ΪFeS2��Ϊԭ���Ʊ��Ȼ������壨FeCl3?6H2O���Ĺ����������£�

�ش��������⣺
��1����һ�������£�SO2ת��ΪSO3�ķ�Ӧ�ɱ�ʾΪ2SO2��g��+O2��g��?2SO3��g�����÷�Ӧ��ƽ�ⳣ������ʽΪK= ��������SO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ ��
��2����36.5%���ܶ�Ϊ1.2g?cm-3�������������500mL��9mol/L�����ᣬ���貣�������� ��
A��������B���ձ� C��������ƽ D����Ͳ E.500mL����ƿ F����ͷ�ι�
��3�����ܼ����������о��豣�������������Ŀ���� �� ��
��4��ͨ����������ʱ����������Ҫ��Ӧ�����ӷ���ʽΪ ���ù��̲�����β�����ü���Һ���գ�β������Ⱦ����������Ϊ ��д��ѧʽ����
��5������aΪ �����ˡ�ϴ�ӡ����

�ش��������⣺
��1����һ�������£�SO2ת��ΪSO3�ķ�Ӧ�ɱ�ʾΪ2SO2��g��+O2��g��?2SO3��g�����÷�Ӧ��ƽ�ⳣ������ʽΪK=
��2����36.5%���ܶ�Ϊ1.2g?cm-3�������������500mL��9mol/L�����ᣬ���貣��������
A��������B���ձ� C��������ƽ D����Ͳ E.500mL����ƿ F����ͷ�ι�
��3�����ܼ����������о��豣�������������Ŀ����
��4��ͨ����������ʱ����������Ҫ��Ӧ�����ӷ���ʽΪ
��5������aΪ
���㣺���κ������ε��ת��,��ѧƽ�ⳣ���ĺ���,����һ�����ʵ���Ũ�ȵ���Һ,�Ʊ�ʵ�鷽�������
ר�⣺������Ҫ�Ľ������仯����
��������1�����ݻ�ѧƽ�ⳣ������д������ʽ����ƽ��״̬��������Ũ�ȵ��ݴη��˻����Է�Ӧ��Ũ�ȵ��ݴη��˻��������������������������Һ��Ӧ�������������ƣ�
��2��������Һ���Ƶ��������н��
��3��ԭ���е���������������ɵ��Ȼ�����Ŀ�����ʣ�����������������������ӵ�ˮ�⣬ʹ�������Ԫ��ת��Ϊ�Ȼ�������
��4��������ǿ�����������������������ӣ�β����������ͼ�����жϣ�������������ӷ������Ȼ������壻
��5������Һ��þ����������������ȴ�ᾧ��
��2��������Һ���Ƶ��������н��
��3��ԭ���е���������������ɵ��Ȼ�����Ŀ�����ʣ�����������������������ӵ�ˮ�⣬ʹ�������Ԫ��ת��Ϊ�Ȼ�������
��4��������ǿ�����������������������ӣ�β����������ͼ�����жϣ�������������ӷ������Ȼ������壻
��5������Һ��þ����������������ȴ�ᾧ��
���
�⣺��1����һ�������£�SO2ת��ΪSO3�ķ�ӦΪ2SO2+O2
2SO3���÷�Ӧ��ƽ�ⳣ������ʽΪK=
��
������SO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ��SO2+NaOH=NaHSO3��
�ʴ�Ϊ��K=
��SO2+NaOH=NaHSO3��
��2����36.5%���ܶ�Ϊ1.2g?cm-3�������������500mL��9mol/L�����ᣬ����Ͳ��Ũ���ᡢ���ձ����ܽ⣬�ò���������ע������ƿ���ý�ͷ�ιܶ��ݣ������õ���Ҫ�IJ��������У���Ͳ���ձ�����������500mL����ƿ����ͷ�ιܣ�
�ʴ�Ϊ��ABDEF��
��3�����ܼ����������о��豣�������������Ŀ����ʹ�������ܽ�Ϊ�Ȼ��������������ӵ�ˮ�⣻
�ʴ�Ϊ�������Ԫ�صĽ����ʣ�����Fe3+ˮ�⣻
��4��ͨ����������ʱ������������������Ϊ�����ӣ���������Ҫ��Ӧ�����ӷ���ʽΪ��Cl2+2Fe2+=2Cl-+2Fe3+���ù��̲�����β�����ü���Һ���գ�β������Ⱦ����������Ϊ������������������Һ�лӷ������Ȼ������壻
�ʴ�Ϊ��Cl2+2Fe2+=2Cl-+2Fe3+��Cl2 ��HCl��
��5������Һ��þ����������������ȴ���壬�ʴ�Ϊ������Ũ��������ȴ�ᾧ��
| ||
| �� |
| c2(SO3) |
| c(O2)?c2(SO2) |
������SO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ��SO2+NaOH=NaHSO3��
�ʴ�Ϊ��K=
| c2(SO3) |
| c(O2)?c2(SO2) |
��2����36.5%���ܶ�Ϊ1.2g?cm-3�������������500mL��9mol/L�����ᣬ����Ͳ��Ũ���ᡢ���ձ����ܽ⣬�ò���������ע������ƿ���ý�ͷ�ιܶ��ݣ������õ���Ҫ�IJ��������У���Ͳ���ձ�����������500mL����ƿ����ͷ�ιܣ�
�ʴ�Ϊ��ABDEF��
��3�����ܼ����������о��豣�������������Ŀ����ʹ�������ܽ�Ϊ�Ȼ��������������ӵ�ˮ�⣻
�ʴ�Ϊ�������Ԫ�صĽ����ʣ�����Fe3+ˮ�⣻
��4��ͨ����������ʱ������������������Ϊ�����ӣ���������Ҫ��Ӧ�����ӷ���ʽΪ��Cl2+2Fe2+=2Cl-+2Fe3+���ù��̲�����β�����ü���Һ���գ�β������Ⱦ����������Ϊ������������������Һ�лӷ������Ȼ������壻
�ʴ�Ϊ��Cl2+2Fe2+=2Cl-+2Fe3+��Cl2 ��HCl��
��5������Һ��þ����������������ȴ���壬�ʴ�Ϊ������Ũ��������ȴ�ᾧ��
���������⿼���˻�ѧƽ���ƽ�ⳣ������ʽ��д�����̲����еIJ���Ŀ�ĺͷ�Ӧ����Ӧ����ķ����жϣ�β���ijɷ��жϺʹ�����������Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д� ���������ν�ϵ�д�
���������ν�ϵ�д�
�����Ŀ
 �ռ�ʵ���ҡ��칬һ�š��Ĺ���ϵͳ������������ȼ�ϵ�أ�RFC����RFC��һ�ֽ�ˮ��⼼��������ȼ�ϵ�ؼ������ϵĿɳ���أ���ͼΪRFC����ԭ��ʾ��ͼ���й�˵����ȷ���ǣ�������
�ռ�ʵ���ҡ��칬һ�š��Ĺ���ϵͳ������������ȼ�ϵ�أ�RFC����RFC��һ�ֽ�ˮ��⼼��������ȼ�ϵ�ؼ������ϵĿɳ���أ���ͼΪRFC����ԭ��ʾ��ͼ���й�˵����ȷ���ǣ�������| A��ת��0.1mol����ʱ��a�缫����1.12LH2����״���� |
| B��b�缫�Ϸ����ĵ缫��Ӧ�ǣ�2H2O+2e-=H2��+2OH- |
| C��c�缫�Ͻ��л�ԭ��Ӧ��B����е�H+����ͨ����Ĥ����A�� |
| D��d�缫�Ϸ����ĵ缫��Ӧ�ǣ�O2+4H++4e-=2H2O |
ͬ��ͬѹ�£���������ͬ�İ�������ϩ�����ǵģ�������
| A�������ͬ | B���ܶ���ͬ |
| C��ԭ����Ŀ��ͬ | D��������ͬ |
��NAΪ�����ӵ�������������������ȷ���ǣ�������
| A���ڳ��³�ѹ�£�11.2 L N2���еķ�����Ϊ0.5 NA |
| B���ڳ��³�ѹ�£�1 mol Ne���е�ԭ����ΪNA |
| C��1 L 1 mol/L������Һ����������Ϊ2NA |
| D��18 gˮ�������ĵ�����Ϊ8NA |
һ���¶��£��ڼס��ҡ��������ĸ������ܱ�������Ͷ��SO2��g����O2��g��������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ�������ж��У�����ȷ���ǣ�������
| �� | �� | �� | �� | ||
| �ܱ��������/L | 2 | 2 | 2 | 1 | |
| ��ʼ���ʵ��� | n��SO2��/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n��O2��/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| SO2��ƽ��ת����/% | 80 | ��1 | ��2 | ��3 | |
| A�����з�Ӧ��ƽ�ⳣ���붡�з�Ӧ��ƽ�ⳣ����� |
| B�����¶��£����з�Ӧ��ƽ�ⳣ��KΪ200 |
| C��SO2��ƽ��ת���ʣ���2����1 |
| D��������SO3�����ʵ���Ũ�ȣ���=�� |
�����������и�����������Һ�У��ܴ���������������ǣ�������
| A����ʹpH��ֽ�ʺ�ɫ����Һ��CH3COOH��NH4+��I-��NO3- |
| B��������������H2����Һ��K+��Mg2+��SO42-��HCO3- |
| C��c��Fe3+��=0.1mol?L-1����Һ��H+��Al3+��Cl-��SCN- |
| D��pH=14����Һ��Na+��NH3?H2O��SiO32-��NO3- |
����ָ����Ӧ�����ӷ���ʽ��ȷ���ǣ�������
| A���Ȼ�����Һ�м�������İ�ˮ��Al3++4 NH3?H2O=AlO2-+4 NH4+ |
| B��ϡ�����м���������ۣ�Fe+4H++NO3-=Fe3++NO��+2H2O |
| C��̼���Ƶ�ˮ�⣺CO32-+2H2O�TH2CO3+2OH- |
| D��ʯ��ˮ�м������С�մ���Һ��Ca2++2OH-+2HCO3-=CaCO3��+CO32-+H2O |
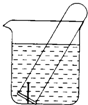 ��ͼˮ�����Թ�����һö���������������۲죺
��ͼˮ�����Թ�����һö���������������۲죺