题目内容
 (2012?潍坊一模)黄铁矿(Fe2S,其中S为-1价)是工业生产硫酸的重要原料.FeS2在高温下与氧气反应:3FeS2+8O2
(2012?潍坊一模)黄铁矿(Fe2S,其中S为-1价)是工业生产硫酸的重要原料.FeS2在高温下与氧气反应:3FeS2+8O2
| ||
(1)若有标准状况22.4L O2参加反应,转移电子的物质的量为
4mol
4mol
.(2)已知1g的二氧化硫催化氧化生成气态三氧化硫,放出热量1.536kJ,请写出该反应的热化学方程式:
2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ/mol
2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ/mol
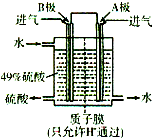
.(3)某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触.请问:B极的电极反应式为
SO2-2e-+2H2O═SO42-+4H+
SO2-2e-+2H2O═SO42-+4H+
;溶液中H+的移动方向由B
B
极到A
A
极;电池总反应式为2SO2+O2+2H2O=2H2SO4
2SO2+O2+2H2O=2H2SO4
.分析:(1)根据氧气和转移电子之间的关系式计算;
(2)根据1g二氧化硫被氧化生成三氧化硫放出的热量计算2mol二氧化硫被氧化放出的热量,再根据热化学反应方程式的书写规则书写;
(3)本题为SO2与O2反应生成SO3,SO3再与水化合生成硫酸,根据硫酸的出口判断正负极,负极发生氧化反应,正极发生还原反应,原电池放电时,电解质溶液中阳离子向正极移动.
(2)根据1g二氧化硫被氧化生成三氧化硫放出的热量计算2mol二氧化硫被氧化放出的热量,再根据热化学反应方程式的书写规则书写;
(3)本题为SO2与O2反应生成SO3,SO3再与水化合生成硫酸,根据硫酸的出口判断正负极,负极发生氧化反应,正极发生还原反应,原电池放电时,电解质溶液中阳离子向正极移动.
解答:解:(1)设转移电子的物质的量是x,
3FeS2+8O2
6SO2+Fe3O4 转移电子
(8×22.4)L 32mol
22.4L x
x=
=4mol,
答:转移电子的物质的量是4mol;
(2)1g二氧化硫被氧化生成三氧化硫放出热量1.536kJ,则2mol二氧化硫被氧化生成三氧化硫放出热量
=196.6kJ,所以其热化学反应方程式为:2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ/mol,
故答案为:2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ/mol;
(3)该原电池中,负极上失电子被氧化,所以负极上投放的气体是二氧化硫,二氧化硫失电子和水反应生成硫酸根离子和氢离子,正极上投放的气体是氧气,正极上氧气得电子和氢离子反应生成水,根据硫酸和水的出口方向知,B极是负极,A极是正极,所以B极上的电极反应式为:SO2-2e-+2H2O═SO42-+4H+,原电池放电时,氢离子由负极B移向正极A,所以其电池反应式为:2SO2+O2+2H2O=2H2SO4,
故答案为:SO2-2e-+2H2O═SO42-+4H+;B;A;2SO2+O2+2H2O=2H2SO4.
3FeS2+8O2
| ||
(8×22.4)L 32mol
22.4L x
x=
| 32mol×22.4L |
| (8×22.4)L |
答:转移电子的物质的量是4mol;
(2)1g二氧化硫被氧化生成三氧化硫放出热量1.536kJ,则2mol二氧化硫被氧化生成三氧化硫放出热量
| 2mol×1.536kJ | ||
|
故答案为:2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ/mol;
(3)该原电池中,负极上失电子被氧化,所以负极上投放的气体是二氧化硫,二氧化硫失电子和水反应生成硫酸根离子和氢离子,正极上投放的气体是氧气,正极上氧气得电子和氢离子反应生成水,根据硫酸和水的出口方向知,B极是负极,A极是正极,所以B极上的电极反应式为:SO2-2e-+2H2O═SO42-+4H+,原电池放电时,氢离子由负极B移向正极A,所以其电池反应式为:2SO2+O2+2H2O=2H2SO4,
故答案为:SO2-2e-+2H2O═SO42-+4H+;B;A;2SO2+O2+2H2O=2H2SO4.
点评:本题考查物质的量的有关计算、热化学反应方程式的书写、原电池原理,注意原电池放电时,电解质溶液中阴阳离子的移动方向,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (2012?潍坊一模)反应N2O4(g)?2NO2(g)△H=57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示.下列说法正确的是( )
(2012?潍坊一模)反应N2O4(g)?2NO2(g)△H=57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示.下列说法正确的是( ) ,
,