题目内容
[实验化学]
邻叔丁基对苯二酚(TBHQ) 是一种新颖的食品抗氧剂,其制备原理为:

实验过程中的主要步骤如下:

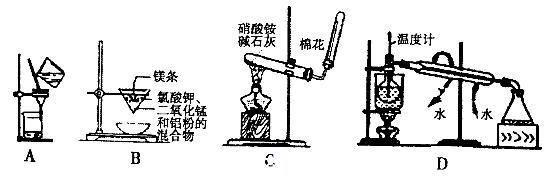
步骤1.向三口烧瓶中加入5.5g对苯二酚,5.OmL浓磷酸及20mL二甲苯(装置如图所示),启动搅拌器。
步骤2.缓缓加热到100-110°C,慢慢滴加7.5mL叔丁醇和5mL二甲苯组成的溶液,30-60min内滴完。
步骤3.升温到135-140°C,恒温回流2.5h。
步骤4.将反应液冷却到120°C,直到反应完成
步骤5.将反应液倒入烧杯,并用热水洗涤三口烧瓶,洗液并入烧杯中。
步骤6.冷却结晶,抽滤,回收滤液中的二甲苯和磷酸
步骤7.用二甲苯重结晶、脱色、冷水洗涤、干燥
(1)磷酸在实验中的作用是 。
(2)本实验中二甲苯的作用是 。
(3)步骤4中反应完成的标志是 。
(4)步骤7脱色时,可用的脱色剂是 。
(5)对合成得到的产品表征,还需要的主要现代分析仪器是 、 。
邻叔丁基对苯二酚(TBHQ) 是一种新颖的食品抗氧剂,其制备原理为:

实验过程中的主要步骤如下:

步骤1.向三口烧瓶中加入5.5g对苯二酚,5.OmL浓磷酸及20mL二甲苯(装置如图所示),启动搅拌器。
步骤2.缓缓加热到100-110°C,慢慢滴加7.5mL叔丁醇和5mL二甲苯组成的溶液,30-60min内滴完。
步骤3.升温到135-140°C,恒温回流2.5h。
步骤4.将反应液冷却到120°C,直到反应完成
步骤5.将反应液倒入烧杯,并用热水洗涤三口烧瓶,洗液并入烧杯中。
步骤6.冷却结晶,抽滤,回收滤液中的二甲苯和磷酸
步骤7.用二甲苯重结晶、脱色、冷水洗涤、干燥
(1)磷酸在实验中的作用是 。
(2)本实验中二甲苯的作用是 。
(3)步骤4中反应完成的标志是 。
(4)步骤7脱色时,可用的脱色剂是 。
(5)对合成得到的产品表征,还需要的主要现代分析仪器是 、 。
(1)催化剂
(2)一是作溶剂,稀释叔丁醇,防止局部浓度过高,生成副产物DTBHQ,二是考虑DTBHQ溶于冷的二甲苯,可除去产品中的DTBHQ
(3)不再有回流液
(4)活性炭
(5)红外光谱仪;熔点测定仪
(2)一是作溶剂,稀释叔丁醇,防止局部浓度过高,生成副产物DTBHQ,二是考虑DTBHQ溶于冷的二甲苯,可除去产品中的DTBHQ
(3)不再有回流液
(4)活性炭
(5)红外光谱仪;熔点测定仪
试题分析:(1)由方程式知,H3PO4作催化剂作用。(2)使用二甲苯是为了减少副产物的发生,或是提高产率。(3)当不再出现回流液时,说明反应不再发生。(4)活性炭可以作为脱色剂,去色素。(4)红外光谱可以测定化学键和官能团,熔点测定仪可以确定产物的纯度等。

练习册系列答案
相关题目


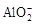 、
、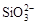 、
、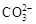 、
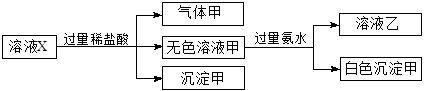
、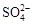 中的若干种离子。某同学对该溶有进行了如下实验:
中的若干种离子。某同学对该溶有进行了如下实验: