题目内容
在100℃时,将0.100mol的N2O4气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如表格:
试填空:
(1)达到平衡时N2O4的转化率为______%,表中c2______c3,a______b (选填“>”“<”“=”).
(2)20s的四氧化二氮的浓度c1=______mol?L-1,在0s~20s内四氧化二氮的平均反应速率为______mol?(L?s)-1;.
(3)若在相同情况下最初向该容器充入的是二氧化氮气体要达到上述同样的平衡状态,二氧化氮的起始浓度是______mol?L-1.
| 时间/s 浓度mol?L-1 |
0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)mol?L-1 | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2)/mol?L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
(1)达到平衡时N2O4的转化率为______%,表中c2______c3,a______b (选填“>”“<”“=”).
(2)20s的四氧化二氮的浓度c1=______mol?L-1,在0s~20s内四氧化二氮的平均反应速率为______mol?(L?s)-1;.
(3)若在相同情况下最初向该容器充入的是二氧化氮气体要达到上述同样的平衡状态,二氧化氮的起始浓度是______mol?L-1.
(1)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,
N2O4

2 NO2,
浓度变化:0.06mol/L 0.120mol/L
所以平衡时N2O4的转化率为
×100%=60%;
c3=0.1mol/L-0.06mol/L=0.04mol/L,
由表可知,40s时,c(N2O4 )=0.050mol/L,
N2O4

2 NO2,
浓度变化:(0.1-0.05)mol/L 0.10mol/L
所以c2=0.10mol/L
所以c2>c3;
60s后反应达平衡,反应混合物各组分的浓度不变,所以a=b.
故答案为:60;>;=
(2)由表可知,20s时,c(NO2 )=0.060mol/L,所以
N2O4

2 NO2,
浓度变化:0.03mol/L 0.060mol/L
所以20s的四氧化二氮的浓度c1=0.1mol/L-0.03mol/L=0.07mol/L;
在0s~20s内四氧化二氮的平均反应速率为v(N2O4)=
=0.0015mol?(L?s)-1.
故答案为:0.07mol/L;0.0015mol?(L?s)-1.
(3)达到上述同样的平衡状态,为等效平衡,按化学计量数换算到N2O4一边,满足c(N2O4)为0.100mol/L.
所以 N2O4

2 NO2,
0.1mol/L 0.20mol/L
故答案为:0.20mol/L
N2O4

2 NO2,
浓度变化:0.06mol/L 0.120mol/L
所以平衡时N2O4的转化率为
| 0.06mol/L |
| 0.1mol/L |
c3=0.1mol/L-0.06mol/L=0.04mol/L,
由表可知,40s时,c(N2O4 )=0.050mol/L,
N2O4

2 NO2,
浓度变化:(0.1-0.05)mol/L 0.10mol/L
所以c2=0.10mol/L
所以c2>c3;
60s后反应达平衡,反应混合物各组分的浓度不变,所以a=b.
故答案为:60;>;=
(2)由表可知,20s时,c(NO2 )=0.060mol/L,所以
N2O4

2 NO2,
浓度变化:0.03mol/L 0.060mol/L
所以20s的四氧化二氮的浓度c1=0.1mol/L-0.03mol/L=0.07mol/L;
在0s~20s内四氧化二氮的平均反应速率为v(N2O4)=
| 0.03mol/L |
| 20s |
故答案为:0.07mol/L;0.0015mol?(L?s)-1.
(3)达到上述同样的平衡状态,为等效平衡,按化学计量数换算到N2O4一边,满足c(N2O4)为0.100mol/L.
所以 N2O4

2 NO2,
0.1mol/L 0.20mol/L
故答案为:0.20mol/L

练习册系列答案
相关题目
在100℃时,将0.40molNO2气体充入2L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
|
 氮可形成多种氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互转化.
氮可形成多种氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互转化.(1)对反应2NO2(g)?N2O4(g)△H=-57.2kJ?mol-1
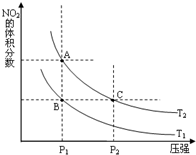
①在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.T1
②A、C两点气体的平均相对分子质量:A
(2)在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
②该条件下平衡常数K的值为
③若其他条件不变,下列既能加快正反应速率又能提高NO2转化率的措施是
④若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始的物质的量是
⑤若其它条件不变,只将容器改为带活塞的恒压容器,则平衡时N2O4的量
 在100℃时,将0.40mol二氧化氮气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
在100℃时,将0.40mol二氧化氮气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
 非金属元素氮有多种氧化物,如NO、NO2、N2O4等.
非金属元素氮有多种氧化物,如NO、NO2、N2O4等.