题目内容
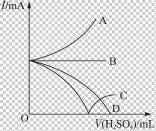
向盛有一定量Ba(OH)2的溶液里逐滴加入稀H2SO4,直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)近似地用如图中曲线表示的是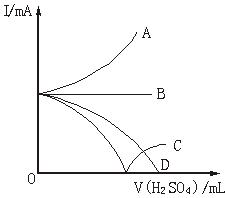
解析:溶液的导电能力由溶液中自由移动的离子的浓度大小决定。Ba(OH)2是强电解质,未加H2SO4溶液时,溶液有一定的导电能力,但随着H2SO4的加入,因发生反应Ba(OH)2+H2SO4===BaSO4↓+2H2O,而使混合溶液中离子浓度减小,当Ba(OH)2和H2SO4完全反应时,溶液的导电能力几乎为零,再继续滴加H2SO4,H2SO4是强电解质,又电离出H+和![]() ,溶液的导电能力又增强。
,溶液的导电能力又增强。
答案:C

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
 向盛有一定量的Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)近似的用下图中的曲线表示是( )
向盛有一定量的Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)近似的用下图中的曲线表示是( )