题目内容
实验室中下列实验药品的保存和事故处理的方法中,不正确的是( )
| A、不慎把浓硫酸沾在手上,立即用干布拭去,再用水冲洗 |
| B、铝条和铝片不需要采用密封保护的方法 |
| C、氢氟酸或浓硝酸存放在带橡皮塞的棕色玻璃瓶中 |
| D、氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中 |
考点:化学实验安全及事故处理
专题:化学实验基本操作
分析:A.浓硫酸具有腐蚀性,浓硫酸和水反应放出大量热量;
B.铝在空气中写出致密的保护膜;
C.氢氟酸和二氧化硅反应,硝酸腐蚀橡胶;
D.氯水和硝酸银见光易分解,要密封保存在棕色瓶中.
B.铝在空气中写出致密的保护膜;
C.氢氟酸和二氧化硅反应,硝酸腐蚀橡胶;
D.氯水和硝酸银见光易分解,要密封保存在棕色瓶中.
解答:
解:A.浓硫酸具有腐蚀性,浓硫酸和水反应放出大量热量,故A正确;
B.铝在空气中写出致密的保护膜,阻止铝的进一步氧化,故B正确;
C.氢氟酸和二氧化硅反应,硝酸腐蚀橡胶,故C错误;
D.氯水和硝酸银见光易分解,要密封保存在棕色瓶中,故D正确;
故选C.
B.铝在空气中写出致密的保护膜,阻止铝的进一步氧化,故B正确;
C.氢氟酸和二氧化硅反应,硝酸腐蚀橡胶,故C错误;
D.氯水和硝酸银见光易分解,要密封保存在棕色瓶中,故D正确;
故选C.
点评:本题考查化学实验基本操作,难度不大,注意基础知识的积累.

练习册系列答案
 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
盐酸与锌反应时,若加入少量可溶性的盐(CH3COO)2Cu,对该反应的反应速率产生的影响是( )
| A、增大 | B、减少 |
| C、不能确定 | D、无影响 |
在盛稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )
| A、溶液中的SO42-移向正极,一段时间后正极附近的SO42-浓度增大 |
| B、铜片是正极,锌片是负极 |
| C、正极吸收H2 |
| D、正极吸收O2 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1mol氦气中有2NA个氦原子 |
| B、2L 0.3mol/L Na2SO4溶液中含0.6NA个Na+ |
| C、14g氮气中含NA个氮原子(氮的相对原子质量为14) |
| D、18g水中所含的电子数为8NA |
 Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图所示,电解总反应为:2Cu+H2O
Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图所示,电解总反应为:2Cu+H2O
| ||
| A、石墨电极上产生氢气 |
| B、铜电极发生的电极反应为:2Cu-2e-+2OH-?Cu2O+H2O |
| C、铜电极接直流电源的正极 |
| D、当有0.1mol电子转移时,有0.1mol Cu2O生成 |
把2.5mol A和2.5mol B混合通入容积为1L的密闭容器里发生如下反应:3A(g)+B(g)?x C(g)+2D(g),容器里的压强逐渐降低,经5s后保持不变.在此5s内C的平均反应速率为0.1mol?L-1?s-1.则下列的说法中正确的是( )
| A、达平衡时,A的物质的量浓度2.0 mol/L |
| B、达平衡时,B的转化率20% |
| C、此5s内D的平均反应速率为0.2 mol?L-1?min-1 |
| D、x≥3 |
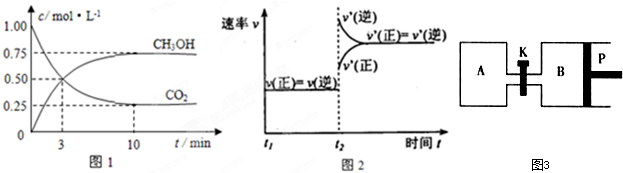
 按如图装置进行实验,并回答下列问题:
按如图装置进行实验,并回答下列问题: