题目内容
12.观察如下反应,总结规律,然后完成下列问题:①Al(OH)3+H2O?Al(OH)4-+H+;
②NH3+H2O?NH4++OH-
(A)已知B(OH)3是一元弱酸,试写出其电离方程式B(OH)3+H2O?B(OH)4-+H+;
(B)已知N2H4是二元弱碱,试写出其二步电离方程式N2H5++H2O?N2H62++OH-.
分析 (A)B(OH)3是一元弱酸,类似Al(OH)3的电离,B(OH)3应是与水作用也生成生成酸根离子与氢离子;
(B)N2H4是二元弱碱,其性质与氨气相似,第一步电离出1个氢氧根离子和N2H5+,则第二步中N2H5+电离出1个氢氧根离子和N2H62+.
解答 解:(A)B(OH)3是一元弱酸,类似Al(OH)3的电离,B(OH)3应是与水作用也生成生成酸根离子,其电离方程式书为:B(OH)3+H2O?B(OH)4-+H+;
故答案为:B(OH)3+H2O?B(OH)4-+H+;
(B)N2H4是二元弱碱,其电离分步进行,第一步N2H4部分电离出OH-、N2H5+,则第二步中N2H5+在溶液中部分电离出出OH-、N2H62+,第二步电离方程式为:N2H5++H2O?N2H62++OH-,
故答案为:N2H5++H2O?N2H62++OH-.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱及电离方式是解题关键,注意对已有知识的迁移应用,类比氢氧化铝的电离方式即可解答,题目难度不大.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
2.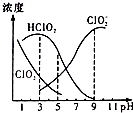 织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.25℃时,各组分含量随pH变化情况如图所示(Cl-没有画出),下列说法错误的是 ( )( )
织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.25℃时,各组分含量随pH变化情况如图所示(Cl-没有画出),下列说法错误的是 ( )( )
 织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.25℃时,各组分含量随pH变化情况如图所示(Cl-没有画出),下列说法错误的是 ( )( )
织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.25℃时,各组分含量随pH变化情况如图所示(Cl-没有画出),下列说法错误的是 ( )( )| A. | 25℃时,HClO2的电离平衡常数的数值Ka=10-6 | |
| B. | 使用该漂白剂的最佳pH为3.0 | |
| C. | 25℃时,等浓度的HClO2溶液和NaClO2溶液等体积混合后,混合溶液中:c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-) | |
| D. | 该温度下NaClO2溶液中:c(Na+)>c(ClO2-)>c(OH-)>c(H+) |
20.有机物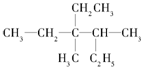 的正确命名为( )
的正确命名为( )
 的正确命名为( )
的正确命名为( )| A. | 3-甲基4,4-二乙基戊烷 | B. | 3-甲基3,4-二乙基戊烷 | ||
| C. | 4-甲基2,2-二乙基己烷 | D. | 3,4-二甲基3-乙基己烷 |
7.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 1mol•L-1NaCl溶液中含有NA个Na+ | |
| B. | 25℃,101kPa,64gSO2中含有的原子数为3NA | |
| C. | 在常温常压下,22.4LCl2含有的分子数为NA | |
| D. | 标准状况下,11.2LCCl4含有的分子数为0.5NA |
17.某化合物有碳、氢、氧三种元素组成,其红外光谱图有C-H键、O-H键、C-O键的振动吸收,该有机物的相对分子质量是60,则该有机物的结构简式( )
| A. | CH3CH2OCH3 | B. | CH3CH(OH)CH3 | C. | CH3CH2 CH2CH2OH | D. | CH3CH2CHO |
4.NA为阿伏加德罗常数的值.下列说法中,正确的是( )
| A. | 17 g甲基(-14CH3)所含电子数为10NA | |
| B. | 标准状况下,0.56L丙烷中含有共价键的数目为0.2NA | |
| C. | 在反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,每生成3molCl2转移的电子数为5NA | |
| D. | 0.1mol9038Sr原子中含中子数为3.8NA |
2.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1 mol D2O所含质子数为12 NA | |
| B. | 1 mol C16H34中的极性键数为34 NA | |
| C. | 10 g 氖气所含原子数为NA | |
| D. | 22.4 L正戊烷含氢原子数为12 NA |
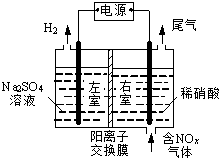 电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).
电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).