题目内容
已知化合物甲和乙都不溶于水,甲可溶于质量分数大于或等于98%的浓硫酸,而乙不溶.现有一份甲和乙的混合物样品,通过实验进行分离可得到固体甲(实验中使用的过滤器是用于过滤强酸性液体的耐酸过滤器).
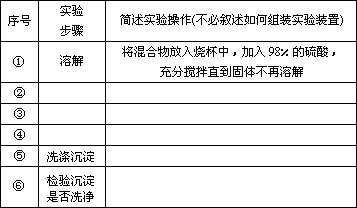
请填写表中空格,完成由上述混合物得到固体甲的实验设计.
解析:
|
答案:②过滤,将混合物沿玻璃棒倒入耐酸过滤器中,用烧杯收集滤液得甲的浓硫酸溶液 ③溶解,将甲的浓硫酸溶液沿器壁慢慢倒入烧杯内的蒸馏水中,用玻璃不断棒搅拌,使液体混合均匀并冷却至室温 ④过滤,将混合物沿着玻璃棒倒入过滤器中,用烧杯收集滤液 ⑤用烧杯向过滤器中加蒸馏水使水面略高于固体,再重复这样的操作两次 ⑥取最后一次洗液约2 mL盛于试管中,向其中加适量的Ba(NO3)2溶液,若没有生成白色沉淀,说明沉淀已洗净 解析:因为甲可溶于ω(H2SO4)≥98%的硫酸,而乙不溶,所以将甲和乙的混合物溶于浓硫酸后再过滤就得甲的硫酸溶液.又因为甲溶于浓硫酸,而不溶于水,所以将甲的浓硫酸溶液加到水中,甲就沉淀析出,此时再过滤就得甲的固体. |
提示:
|
(重点提示)注意洗涤沉淀的操作方法. |

序号 | 实验步骤 | 简述实验操作(不必叙述如何组装实验装置) |
① | 溶解 | 将混合物放入烧杯中,加入98% H2SO4,充分搅拌直到固体不再溶解 |
② |
|
|
③ |
|
|
④ |
|
|
⑤ | 洗涤沉淀 |
|
⑥ | 检验沉淀?是否洗净 |
|
请填写表中空格,完成由上述混合物得到固体甲的实验设计。
序号 | 实验步骤 | 简述实验操作(不必叙述如何组装实验装置) |
① | 溶解 | 将混合物放入烧杯中,加入98%的浓H2SO4,充分搅拌直到固体不再溶解 |
② |
|
|
③ |
|
|
④ |
|
|
⑤ | 洗涤沉淀 |
|
⑥ | 检验沉淀是否洗净 |
|
请填写表中空格,完成由上述混合物得到固体甲的实验设计。
序号 | 实验步骤 | 简述实验操作(不叙述如何组装实验装置) |
① | 溶解 | 将混合物放入烧杯中,加入98%硫酸中,充分搅拌直到固体不再溶解 |
② |
|
|
③ |
|
|
④ |
|
|
⑤ | 洗涤沉淀 |
|
⑥ | 检验沉淀是否洗净 |
|
已知化合物甲和乙都不溶于水,甲可溶于质量分数大于或等于98%的硫酸,而乙不溶。现有一份甲和乙的混合物样品,通过实验进行分离,可得到固体甲。(实验中使用的过滤器是用于过滤强酸性液体的耐酸过滤器。)
请填写表中空格,完成由上述混合物得到固体甲的实验设计。
|
序号 |
实验步骤 |
简述实验操作(不必叙述如何组装实验装置) |
|
① |
溶解 |
将混合物放入烧杯中,加入98% H2SO4,充分搅拌直到固体不再溶解。 |
|
② |
|
|
|
③ |
|
|
|
④ |
|
|
|
⑤ |
洗涤沉淀 |
|
|
⑥ |
检验沉淀 是否洗净 |
|