��Ŀ����
����Ŀ������ͼʾ���Ӧ��������������ǣ� ��
A.
��ʾ10 mL 0.01molL��1KMnO4������Һ�������0.1molL��1 H2C2O4��Һ���ʱ��n��Mn2+����ʱ��ı仯��Mn2+�Ը÷�Ӧ�д����ã�
B.
��ʾij���ȷ�Ӧ�ֱ����С�����������·�Ӧ�����е������仯
C.
��ʾʾ���������������Ƶ�ƫ��������Һ�еμ��������ó������ʵ�������������Ĺ�ϵ
D.
��ʾ��NH4Al��SO4��2��Һ����ε���Ba��OH��2��Һ������Ba��OH��2��Һ���V�ı仯�����������ʵ���n�ı仯
���𰸡�C
���������⣺A�����ݷ�Ӧ2MnO4��+5H2C2O4+6H+=2Mn2++10CO2��+8H2O��֪���÷�Ӧ�в����������ӣ������ӶԸ÷�Ӧ���˴����ã����ӿ��˷�Ӧ���ʣ�����ͼ��Ϊ�� 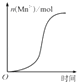 ����A��ȷ��
����A��ȷ��
B����Ӧ������������������������������Ӧ�Ƿ��ȷ�Ӧ����������ή�ͻ�ܣ��ı䷴Ӧ�����ʣ�����Ӧ�Ȳ��ı䣬��B��ȷ��
C���ȷ���NaOH������ķ�Ӧ�����ɳ�����Ȼ����NaAlO2+HCl+H2O=Al��OH��3��+NaCl��Al��OH��3+3HCl=AlCl3+3H2O�������������ܽ�������Ϊ1��3����ͼ������C����
D����ʼ�μ�ͬʱ������ӦΪSO42��+Ba2+=BaSO4����Al3++3OH��=Al��OH��3������Al3+������ȫʱ�����0.03molOH�� �� ������0.015molBa��OH��2 �� �����Ba2+Ϊ0.015mol��SO42��δ��ȫ��������ʱ��Һ��������李�������������ʼ��a���ٵμ�Ba��OH��2 �� ����BaSO4������������ӦΪSO42��+Ba2+=BaSO4����NH4++OH��=NH3H2O�����Գ��������������ӣ���SO42����ȫ����ʱ���������0.02molBa��OH��2 �� ����0.04molOH�� �� Al3+��Ӧ��0.03molOH�� �� ����Al��OH��30.01mol��ʣ��0.01molOH��ǡ����NH4+��ȫ��Ӧ����ʱ��Һ��NH4+��ȫ��Ӧ����ʱ��ҺΪ��ˮ��Һ����a��b�������μ�Ba��OH��2 �� Al��OH��3�ܽ⣬������ӦAl��OH��3+OH��=AlO2��+2H2O���ɷ���ʽ��֪Ҫʹ0.01molAl��OH��3��ȫ�ܽ⣬���ټ���0.005molBa��OH��2 �� ��ʱ��ҺΪ��ˮ��ƫ���ᱵ��Һ����b��c������D��ȷ��
��ѡC��
�����㾫����������Ҫ�����˷�Ӧ�Ⱥ��ʱ�����֪ʶ�㣬��Ҫ�����ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�Ȳ�����ȷ�����⣮



