题目内容
下列化学方程式表示的制备钠的化合物的实验方案,哪些是切实可行的?说明理由。(1)制备Na2O:4Na+2O2===2Na2O2
(2)制备Na2O2:4Na+2O2![]() 2Na2O2
2Na2O2
(3)制备Na2O:2NaNO2+6Na===4Na2O+N2↑
(4)制备Na2O2:2Na2O+O2===2Na2O2
(5)制备Na2O:Na2O2+2Na===2Na2O
(1)不可行 (2)(3)(4)(5)切实可行。
碱金属的氧化物(除锂外)必须用间接的方法制得,这是因为Na2O不稳定,它会跟O2反应:2Na2O+O2===2Na2O2。工业上制备Na2O的方法有(3)和(5);制备Na2O2的方法有(2)和(4)。其中方法(2)的具体操作是:将钠加热至熔化,通入一定量的除去CO2的干燥空气维持温度在453&473 K之间钠即被氧化成Na2O,进而增加空气流量升温到573&673 K即可制得Na2O2。

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目

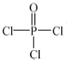 )与季戊四醇(
)与季戊四醇(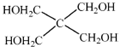 )以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体.季戊四醇与X 的核磁共振氢谱如图所示.
)以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体.季戊四醇与X 的核磁共振氢谱如图所示.
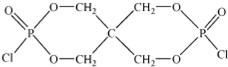
 Zn(OH)2+2Ag
Zn(OH)2+2Ag 2PbSO4+2H2O:
2PbSO4+2H2O: