题目内容
有关溶液描述下列说法正确的是( )
分析:根据溶液中离子的水解与电解质的电离来分析离子浓度的大小及溶液中微粒的种类,并利用溶液的PH值来分析溶液的酸碱性,利用溶液中的溶质来分析稀释后溶液pH的变化.
解答:解:A、25℃时0.08mol/L二元酸H2A的溶液中pH=1,则酸第一步完全电离,第二步是不完全电离,在NaHA溶液中HA-的电离大于HA-的水解,则c(A2-)>c(H2A),故A错误;
B、浓度相同的①NH4HSO4、②(NH4)2CO3、③CH3COONH4溶液中,若设浓度为1mol/L,则②中1mol/L<c(NH4+)<2mol/L,则c(NH4+)②>①>③,即②的c(NH4+)最大,故B错误;
C、若为常温下pH=7的氯化钠溶液,则加水稀释,pH不变,若溶液为酸性或碱性则稀释时pH可能增大或减小,故C错误;
D、在①CH3COONa中存在四种离子和两种分子,②NH3的水溶液中有三种离子和三种分子,③K2S溶液中五种离子和2种分子,则③含粒子种类最多且有7种粒子,故D正确;
故选D.
B、浓度相同的①NH4HSO4、②(NH4)2CO3、③CH3COONH4溶液中,若设浓度为1mol/L,则②中1mol/L<c(NH4+)<2mol/L,则c(NH4+)②>①>③,即②的c(NH4+)最大,故B错误;
C、若为常温下pH=7的氯化钠溶液,则加水稀释,pH不变,若溶液为酸性或碱性则稀释时pH可能增大或减小,故C错误;
D、在①CH3COONa中存在四种离子和两种分子,②NH3的水溶液中有三种离子和三种分子,③K2S溶液中五种离子和2种分子,则③含粒子种类最多且有7种粒子,故D正确;
故选D.
点评:本题考查溶液中的电离和水解,学生明确电离与水解的趋势大小及相互影响是解答本题的关键,并注意盐类水解的程度、弱电解质的电离程度小来分析解答即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 《物质结构与性质》
《物质结构与性质》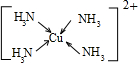
 ,下列说法正确的是
,下列说法正确的是 SO2Cl2(l)△H=-97.3kJ?mol-1
SO2Cl2(l)△H=-97.3kJ?mol-1