题目内容
| A、溶液的导电性与溶液中离子的浓度有关 | B、溶液的导电性与溶液中离子的种类有关 | C、溶液的导电性与溶液中离子的种类和数目有关 | D、往氢氧化钡溶液中滴加盐酸与滴加硫酸时现象相同 |
B.溶液的导电性与溶液中离子浓度有关,与溶液中离子种类无关,故B错误;
C.不知道溶液的体积,溶液中离子的浓度大小无法判断,无法判断溶液导电性强弱,故C错误;
D.往氢氧化钡溶液中滴加硫酸至过量,会生成难溶的硫酸钡和难电离的水,所以导电性会先减弱,硫酸过量之后,导电性又增强,所以,灯泡的明亮度变化是:明→暗→明,而往氢氧化钡溶液中滴加盐酸,生成的是易溶易电离的氯化钡,所以,溶液导电能力一直很强,灯泡一直明亮,故D错误.
故选A.

某化学探究性学习小组在探究溶液导电性的实验中发现:往氢氧化钡溶液中滴加硫酸至过量,灯泡的明亮度变化是:明→暗→明,而向盐酸溶液中加入少量氢氧化钠固体灯泡的明亮程度没明显变化,他们由此得到了如下一些结论,其中合理的是 ( )
| A.溶液的导电性与溶液中离子的浓度有关 |
| B.溶液的导电性与溶液中离子的种类有关 |
| C.溶液的导电性与溶液中离子的种类和数目有关 |
| D.往氢氧化钡溶液中滴加盐酸与滴加硫酸时现象相同 |
为检验一批因露置而部分变质的Ba(OH) 2药品的成分,某化学探究性学习小组设计了方案对其进行分析:将20.45g药品分成五等分,逐渐加入100mL1 mol/L的盐酸中,并充分搅拌,测得生成气体的体积(已换算为标准状况下)、剩余固体的量与固体加入量的关系如图所示。考虑到某地附近为硫酸工业区,该小组同学判断此药品可能含三或四种成分。
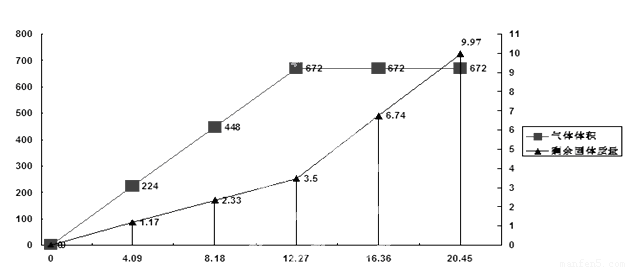
(1) 写出硫酸工业尾气与过量的Ba(OH) 2反应的离子方程式:????????????????????????
(2)提出以下三种合理假设:(已知在空气中Ba(OH) 2很难生成酸式盐)
假设一:药品成分为Ba(OH) 2和BaSO4、BaSO3;假设二:药品成分为Ba(OH) 2和________________;
假设三:药品成分为Ba(OH) 2和________________。
(3)实验验证:为确定该药品的成分,该小组利用上述实验中生成的气体,选择适当的试剂进行探究,请设计合理方案填入下表:
实验操作 | 预期实验现象和结论 |
| 若____________________,假设一成立;
若____________________,假设二成立;
若____________________,假设三成立。 |
(4)问题讨论:若经试验验证,此药品为四种成分混合物,该小组同学认为由上述曲线可知,当所加固体质量为12.27 g时,药品成分与盐酸刚好完全反应,你认为该组同学的判断是否正确______。(填“是”或者“否”)